题目内容
精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
【物质制备】利用绿矾制备精还原铁粉的工艺流程如下:
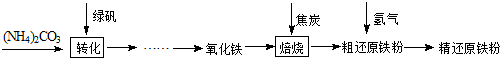
FexOy+yH2 xFe+yH2O Fe3C+2H2
xFe+yH2O Fe3C+2H2 3Fe+CH4粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为: .
3Fe+CH4粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为: .
(1)写出焙烧中氧化铁与CO反应的化学方程式 .
(2)焙烧中加焦炭的作用除了可以作燃料提供反应所需高温外,还能 .
【含量测定】甲同学为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按如下装置进行实验.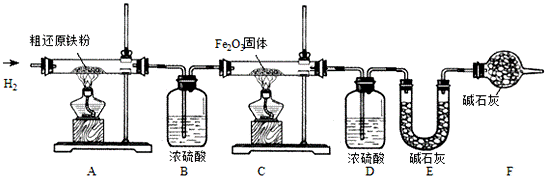
已知:3CH4+4Fe2O3 3CO2+6H2O+8Fe,浓硫酸有吸水性,碱石灰不仅能吸收水而且能吸收CO2.(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响).
3CO2+6H2O+8Fe,浓硫酸有吸水性,碱石灰不仅能吸收水而且能吸收CO2.(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响).
(3)主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入纯净干燥的H2;
③点燃C处酒精灯;
④点燃A 处酒精灯;
⑤分别熄灭A、C处酒精灯;
⑥ ;
⑦再次称量必要装置的质量.
(4)步骤②的目的是 ,验证该步骤目的达到的实验方法是 .
(5)反应后C装置中的现象是 .
(6)装置F的作用是 .
(7)若缺少装置D,则所测氧元素的质量分数将 (“偏大”、“偏小”或“不变”).
(8)实验后,甲同学根据装置 (填A、B、C、D、E、F)的增重分别算得样品中氧和碳元素的质量分数.
(9)乙同学将10.0克粗还原铁粉样品与足量稀盐酸充分反应,经测定共产生0.3克气体.计算该粗还原铁粉样品中铁单质的质量分数.(要求写出计算过程)
答案 解:氢气在高温下还原铁的氧化物、Fe3C的化学方程式为:FexOy+yH2 xFe+yH2O、Fe3C+2H2
xFe+yH2O、Fe3C+2H2 3Fe+CH4.
3Fe+CH4.
故填:FexOy+yH2 xFe+yH2O、Fe3C+2H2
xFe+yH2O、Fe3C+2H2 3Fe+CH4.
3Fe+CH4.
(1)焙烧中氧化铁与CO反应的化学方程式为:Fe2O3+3CO 2Fe+3CO2.
2Fe+3CO2.
故填:Fe2O3+3CO 2Fe+3CO2.
2Fe+3CO2.
(2)焙烧中加焦炭的作用除了可以作燃料提供反应所需高温外,还能和二氧化碳反应生成一氧化碳.
故填:和二氧化碳反应生成一氧化碳.
(3)主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入纯净干燥的H2;
③点燃C处酒精灯;
④点燃A 处酒精灯;
⑤分别熄灭A、C处酒精灯;
⑥继续通H2直至装置冷却;
⑦再次称量必要装置的质量.
故填:继续通H2直至装置冷却.
(4)步骤②的目的是排出装置中的空气,防止加热时发生爆炸,验证该步骤目的达到的实验方法是收集尾气验纯.
故填:排出装置中的空气,防止加热时发生爆炸;收集尾气验纯.
(5)反应后C装置中的现象是红棕色的粉末变成黑色.
故填:红棕色的粉末变成黑色.
(6)装置F的作用是防止空气中的二氧化碳、水蒸气进入E装置.
故填:防止空气中的二氧化碳、水蒸气进入E装置.
(7)若缺少装置D,则所测氧元素的质量分数将不变,这是因为需要的水的质量数据是从B装置得到的.
故填:不变.
(8)实验后,根据装置B的增重可以计算样品中氧元素的质量分数,根据装置E的增重可以计算样品中碳元素的质量分数.
故填:B、E.
(9)解:设该粗还原铁粉样品中铁单质的质量分数为x,
Fe+2HCl═FeCl2+H2↑,
56 2
10.0g×x 0.3g
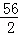 =
= ,
,
x=84%,
答:该粗还原铁粉样品中铁单质的质量分数为84%.

 名校课堂系列答案
名校课堂系列答案对下列化学用语中“2”的说法正确的是( )
①2O3  ②2N ③N2 ④2NO3- ⑤Mg2+ ⑥Mg ⑦H2O
②2N ③N2 ④2NO3- ⑤Mg2+ ⑥Mg ⑦H2O
A.表示分子中原子个数的是③⑦
B.表示离子所带电荷数的是⑤⑥
C.表示离子个数的是④⑤
D.表示分子个数的是①②
如图是某化肥包装袋上的部分说明:
| 碳酸氢铵 化学式:NH4HCO3 净重:50 kg 含氮量:≥16% 注意事项:密封保存 防潮防晒 …… |
(1)碳酸氢铵保存时注意事项是 ;
(2)将碳酸氢铵和氢氧化钙混合研磨就会发生反应,并可闻到刺激性气味。请写出 该反应的化学方程式 ;
该反应的化学方程式 ;
闻到的刺激性气味的气体是氨气,它能使湿润的红色石蕊试纸变 色。



 锈的有效措施是 。
锈的有效措施是 。