题目内容
小明同学在课后练习时遇到下面的一个问题:
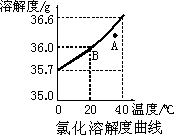
如下图是氯化钠的溶解度曲线,其中A点所示溶液为某温度下氯化钠的________(选填“饱和”或“不饱和”)溶液.
解析:
|
A点溶液是不是饱和溶液呢?小明同学决定实际探究一下. 首先,小明同学对A点所表示的溶液进行了一番研究.根据对溶解度曲线的理解,他认为此点的溶液应该是用100 g水溶解36.3 g氯化钠所配制成的.小丹同学补充说:“还需要知道是什么温度吧?”此观点得到小明和其他同学的支持,他们从图中得出A点温度为38℃.有同学提出:此点的溶液也可以用10 g水溶解3.63 g的氯化钠来配制.同学们经过一番激烈的争论,最后达成共识:此建议理论上是可行的,因为溶解度曲线上的点可以理解为100 g水所溶解溶质的最大量,换个说法即为溶质与溶剂达到一定的比值,如B点就可以理解为20℃时水与氯化钠的质量比为100∶36,当然也可以是10∶3.6.但由于3.63 g氯化钠无法用托盘天平称得,所以,大家还是同意选择在38℃下用100 g水溶解36.3 g氯化钠来配制A点溶液. 实验过程: 1.A点溶液的配制.把开水倒入水槽、烧杯,冷却至38℃,如图所示.加入称量好的36.3 g氯化钠,搅拌至完全溶解.
2.取少量氯化钠,加入到已配制的溶液中,继续搅拌. 3.观察到所加的氯化钠明显减少. 结论与评价: 1.根据观察到氯化钠又被溶解,说明原溶液(A点溶液)为不饱和溶液. 2.放在水槽中进行实验,可使溶液温度不会太快降低. 3.加入少量的氯化钠时未能全部溶解的原因,可能是加入的量有点多.但是,最终氯化钠的质量有所减少应该能说明原来的溶液未达到饱和. 4.溶解度曲线上的点(如B点)为该温度下的饱和溶液,此时溶质与水的质量比应该为:溶解度∶100;而溶解度曲线下方的点所表示的溶液应为不饱和溶液(如题中的A点溶液). 5.由于氯化钠的溶解能力受温度影响不大,所以,此次探究若用硝酸钾等溶解度受温度影响较大的物质进行,效果会更加明显. 联想与拓展: 1.若保持温度不变,向A点溶液中加入适量氯化钠,溶液可变成饱和溶液;恒温蒸发部分水分也能成为饱和溶液. 2.降温至20℃时,A点溶液可以变成B点溶液. 3.你能把B点所表示的溶液变成A点所表示的溶液吗? |