题目内容
13.完成下列化学方程式: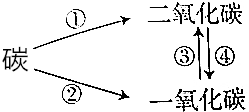
①C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;②2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO;③2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;④2CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:①碳在空气中充分燃烧生成二氧化碳,反应的化学方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
②碳在空气中不充分燃烧生成二氧化碳,反应的化学方程式为:2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO.
③一氧化碳燃烧生成二氧化碳,反应的化学方程式为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
④二氧化碳与碳在高温下反应生成一氧化碳,反应的化学方程式为:2CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
故答案为:①C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;②2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO;③2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;④2CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
1.下列反应的生成物全部为氧化物的分解反应是( )
| A. | 氯酸钾和二氧化锰共热 | B. | 铜绿受热 | ||
| C. | 甲烷燃烧 | D. | 氧化汞受热分解 |
15.下列实验现象的描述中,不正确的是( )
| A. | 铁丝在空气中燃烧:火星四射,生成黑色固体 | |
| B. | 木炭在氧气中燃烧:发出白光 | |
| C. | 镁带在空气中燃烧:发出耀眼白光,生成白色粉末 | |
| D. | 硫在氧气中燃烧:产生明亮的蓝紫色火焰 |
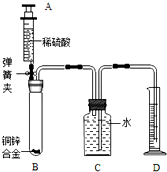 某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)探究过程如下:
某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)探究过程如下: .
.