题目内容
18.科学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:查资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其他成分遇到盐酸时无气体产生.
牙膏样品中碳酸钙的定量测定:取适量牙膏样品,利用右图所示装置进行实验(图中夹持仪器略去),充分反应后,测定C装置中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.请依据实验过程回答下列问题:
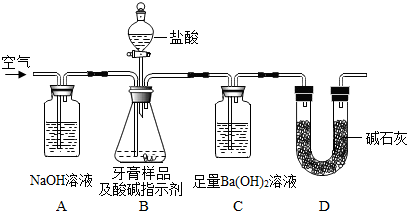
(1)实验过程中需持续缓缓通入空气,其目的是把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收.
(2)有人认为不必测定C装置中生成的BaCO3质量,只要测定C装置在吸收CO2前后的质量,同样可以算出碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是B中的水蒸气、氯化氢气体等进入装置C中.
(3)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g.则样品中碳酸钙的质量分数为多少?
分析 (1)实验通过C装置生成的碳酸钡的质量测定二氧化碳的质量,进而计算牙膏中碳酸钙的质量分数.装置中残留部分二氧化碳,不能被完全吸收,导致测定的碳酸钡的质量偏小;
(2)装置B中的水蒸气和氯化氢气体会进入装置C中;
(3)根据碳酸钙与盐酸反应生成二氧化碳,二氧化碳与氢氧化钡生成碳酸钡沉淀可建立碳酸钙与碳酸钡的关系式,利用题干中的质量关系解决即可;
解答 解:(1)装置中残留部分二氧化碳,不能被完全吸收,导致测定的碳酸钡的质量偏小,持续缓缓通入空气的作用为:把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收,
故答案为:把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收;
(4)B中的水蒸气、氯化氢气体等进入装置C中,导致测定二氧化碳的质量偏大,测定的碳酸钙的质量偏大,碳酸钙的质量分数偏高.
故答案为:B中的水蒸气、氯化氢气体等进入装置C中
(3)由于碳酸钙与盐酸反应生成二氧化碳,二氧化碳与氢氧化钡生成碳酸钡沉淀的方程式分别是:CaCO3+2HCl═CaCl2+H2O+CO2↑;Ba(OH)2+CO2═BaCO3↓+H2O,所以可建立CaCO3→CO2→BaCO3的关系式;
设碳酸钙的质量分数为x
CaCO3→CO2→BaCO3
100 197
8g×x 3.94g
$\frac{100}{8g×x}$=$\frac{197}{3.94g}$
x=25%
故答案为:25%.
点评 本考点属于实验方法和过程的探究,根据物质的化学性质根据所掌握的反应认真分析,既要把握实验设计的每步中的实验目的,又要分析数据的误差.

练习册系列答案
相关题目
9.下列物质能够反应,且没有明显现象的是( )
| A. | 向NaCl溶液中滴加K2SO4溶液 | B. | 向稀盐酸中滴入Ba(OH)2溶液 | ||
| C. | 将浓硫酸加入蒸馏水中并不断搅拌 | D. | 将(NH4)2SO4和熟石灰混合研磨 |
13.下列实验过程中出现的问题,其中原因解释错误的是( )
| 实 验 问 题 | 原 因 | |
| A | “铝箔在氧气中燃烧”的实验过程中,集气瓶底被炸裂. | 集气瓶底部事先没有预留少量水. |
| B | “验证植物呼吸作用产生CO2”的实验中,用澄清石灰水检验时,现象不明显. | 可能是植物样本数量太少 |
| C | 早晨配制的硝酸钾饱和溶液,中午变成了硝酸钾的不饱和溶液. | 温度升高,硝酸钾的溶解度变大 |
| D | “测量小灯泡额定功率”时,正确连接电路后,无论怎样移动滑片,灯泡总是很暗,不能正常发光. | 可能是滑动变阻器的阻值过大 |
| A. | A | B. | B | C. | C | D. | D |
3. 砷化镓是一种光源材料.根据图,下列有关镓的说法不正确的是( )
砷化镓是一种光源材料.根据图,下列有关镓的说法不正确的是( )
 砷化镓是一种光源材料.根据图,下列有关镓的说法不正确的是( )
砷化镓是一种光源材料.根据图,下列有关镓的说法不正确的是( )| A. | 属于金属元素 | B. | 元素符号是Ga | ||
| C. | 相对原子质量为69.72g | D. | 原子的核电荷数是31 |
10.20℃时,将等质量的a、b两种固体,分别加入到盛有lO0g水的烧杯中,充分搅拌后,现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙.下列说法正确的是( )

| A. | 图甲溶液中溶质的质量分数a大于b | B. | 图乙中a、b溶液一定都是饱和溶液 | ||
| C. | 图丙中M表示a的溶解度曲线 | D. | 30℃时a、b溶液溶质质量分数不相等 |
7.下列没有发生化学变化的是( )
| A. |  自制汽水 | B. |  铁生锈条件的探究 | ||
| C. |  酸或碱溶液能改变花的颜色 | D. |  蜡烛燃烧 |
8.密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
下列说法正确的是( )
| 物 质 | A | B | C | D |
| 反应前质量(g) | 19.7 | 8.7 | 31.6 | 0.4 |
| 反应后质量(g) | 待测 | 17.4 | 0 | 3.6 |
| A. | 物质C一定是化合物,物质D可能是单质 | |
| B. | 反应后密闭容器中A的质量为19.7g | |
| C. | 反应过程中,物质B与物质D变化的质量比为87:36 | |
| D. | 反应过程红,物质A与物质C的质量之比为197:316 |
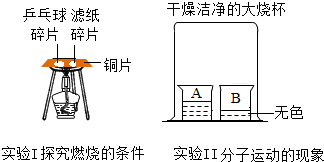 “控制变量”是进行对比实验的重要手段.某同学在学完相关的化学知识后,走进实验室做了如下含有对比思想的化学实验,请你参与并回答下列问题.
“控制变量”是进行对比实验的重要手段.某同学在学完相关的化学知识后,走进实验室做了如下含有对比思想的化学实验,请你参与并回答下列问题.