题目内容
19.硅单质及其化合物应用范围很广.请回答下列问题:(1)制备硅半导体材料必须先得到高纯硅.三氯甲硅烷(SiHCl3)还原法是当前制 备高纯硅的主要方法,生产过程示意图如图:

①写出由纯SiHCl3,制备高纯硅的化学反应方程式_SiHCl3+H2$\frac{\underline{\;高温\;}}{\;}$Si+3HCl.
②整个制备过程必须严格控制无水无氧.SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式SiHCl3+3H2O═H2SiO3↓+H2↑+3HCl;H2还原SiHCl3过程中若混入O2,可能引起的后果是爆炸.
(2)石英砂的主要成分是二氧化硅,高纯度的二氧化硅可用于制造高性能通讯材料----光导纤维.二氧化硅和二氧化碳一样,也能与氢氧化钠溶液生成硅酸钠(其水溶液称水玻璃)和水.请写出二氧化硅与氢氧化钠溶液的化学方程式2NaOH+SiO2=Na2SiO3+H2O.
分析 根据已有的化学方程式的书写的以及物质的性质进行分析解答即可.
解答 解:①SiHCl3,能与氢气高温反应生成硅和氯化氢气体,故填:SiHCl3+H2$\frac{\underline{\;高温\;}}{\;}$Si+3HCl;
②SiHCl3与水反应生成H2SiO3,HCl和氢气,H2还原SiHCl3过程过程中若混入O2,可能引起爆炸,故填:SiHCl3+3H2O═H2SiO3↓+H2↑+3HCl;爆炸;
③氢氧化钠能与二氧化硅反应生成硅酸钠和水,故填:2NaOH+SiO2=Na2SiO3+H2O.
点评 本题考查的是化学方程式的书写的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
10.某学习小组同学用过氧化氢溶液制取氧气.
(1)如表是分解等量的过氧化氢溶液时选用不同催化剂所得到的实验数据:
从上述数据可得出一个结论:在该反应中二氧化锰的催化效果最好.
(2)取含过氧化氢1.7g的溶液,加入适量催化剂充分反应,计算能得到氧气的质量.
(1)如表是分解等量的过氧化氢溶液时选用不同催化剂所得到的实验数据:
| 催化剂(质量均为0.3g) | 新鲜猪肝 | CuCl2 | MnO2 | CuO |
| 收集1L氧气所需的时间(s) | 42 | 650 | 18 | 300 |
(2)取含过氧化氢1.7g的溶液,加入适量催化剂充分反应,计算能得到氧气的质量.
14.下列关于碳和碳的氧化物的说法正确的是( )
| A. | 金刚石和石墨硬度都很大 | |
| B. | 二氧化碳可作为大棚种植农作物的气体肥料 | |
| C. | 二氧化碳和一氧化碳都能灭火 | |
| D. | 一氧化碳可利用水来吸收 |
 能源和环境成为人们日益关注的问题.目前煤炭在我国能源结构中占有的比例最大.
能源和环境成为人们日益关注的问题.目前煤炭在我国能源结构中占有的比例最大.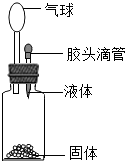 要使如图装置中的小球鼓起来,则使用的固体和液体可以是①②④;
要使如图装置中的小球鼓起来,则使用的固体和液体可以是①②④;
 某化肥包装袋上的部分说明如图所示.请你完成下列各题:
某化肥包装袋上的部分说明如图所示.请你完成下列各题: