题目内容
11.铜是人类最早利用的金属之一.某化学兴趣小组利用废旧电池铜帽(含 Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如下(反应条件已略去):(2Cu+O2+2H2SO4$\frac{\underline{\;加热\;}}{\;}$2CuSO4+2H2O)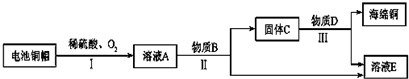
(1)过程Ⅱ中分离操作的名称是过滤.
(2)过程Ⅲ中有气体产生,反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑.该反应属于放热反应(填“放”或“吸”).
(3)A~E 中含铜、锌两种元素的物质有AC(填字母序号).
分析 (1)过滤可以把不溶于水的物质除去;
(2)根据题意可知,锌和稀硫酸反应生成硫酸锌和氢气,铜和氧气、稀硫酸反应生成硫酸铜和水,溶液A中含有硫酸锌和硫酸铜,为了制取海绵铜,并得到硫酸锌溶液,应向溶液A中解过量的锌,锌与硫酸铜反应生成了刘璇新和铜,过滤得到固体C中含有铜和锌,过量的锌再加入质量的硫酸除去;
(3)根据上市过程分析含有铜性元素的物质.
解答 解:由题意可知,锌和稀硫酸反应生成硫酸锌和氢气,铜和氧气、稀硫酸反应生成硫酸铜和水,溶液A中含有硫酸锌和硫酸铜,为了制取海绵铜,并得到硫酸锌溶液,应向溶液A中解过量的锌,锌与硫酸铜反应生成了刘璇新和铜,过滤得到固体C中含有铜和锌,过量的锌再加入质量的硫酸除去.所以:
①由实验的过程可知,过程Ⅱ中分离操作的名称是过滤,可以把铜、锌和硫酸锌溶液分离.
②由上述过程可知,过程Ⅲ中有气体产生,是因为过量的锌和稀硫酸反应生成了氢气,反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑,该反应是放热反应;
③由上述分析可知,溶液A中含有硫酸铜和硫酸锌,因此含有铜、锌两种元素;固体C中含有铜和锌,因此含有铜、锌两种元素.
故答为:(1)过滤;(2)Zn+H2SO4=ZnSO4+H2↑,放;(3)AC.
点评 实验是化学的重要组成部分,正确的实验操作是得出科学结论的前提条件之一,因此要学会设计实验、进行实验、分析实验,为得出正确的结论奠定基础.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
6.下列各组离子在水中一定能大量共存,并形成无色透明溶液的是( )
| A. | NH4+、Na+、NO3- | B. | H+、Ca2+、CO32- | C. | Ba2+、OH-、SO42- | D. | K+、Na+、MnO4- |
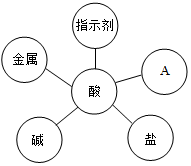 构建知识网络是学习化学的重要方法之一.某同学在学习酸、碱和盐的化学性质后,归纳的知识网络如图,图中“-”两端的物质可以反应.请帮助该同学进行完善和纠正.
构建知识网络是学习化学的重要方法之一.某同学在学习酸、碱和盐的化学性质后,归纳的知识网络如图,图中“-”两端的物质可以反应.请帮助该同学进行完善和纠正.
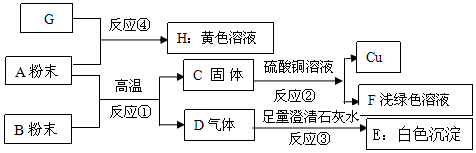
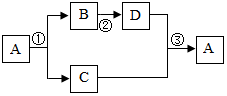 如图所示的转化关系中,A、B、C、D都是初中化学中常见的物质,A是人类赖以生存的一种无色液体,D是一种黑色固体(反应条件、其他反应物及多余的产物均已略去).
如图所示的转化关系中,A、B、C、D都是初中化学中常见的物质,A是人类赖以生存的一种无色液体,D是一种黑色固体(反应条件、其他反应物及多余的产物均已略去).