题目内容
6.某同学在进行化学实验后绘制了如图几个图象,其中不符合事实的是( )| A. | 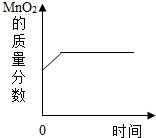 用KClO3和MnO2制取氧气 | |
| B. | 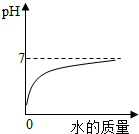 向盐酸中加水 | |
| C. | 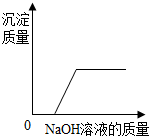 向CuSO4和稀硫酸混合溶液中加入NaOH溶液 | |
| D. |  加热蒸发稀盐酸 |
分析 根据加热氯酸钾和二氧化锰的过程中二氧化锰的作用进行分析,酸中加水则酸被稀释,酸性减弱,氢氧化钠既能和硫酸反应也能和硫酸铜反应,加热蒸发盐酸,则溶质氯化氢的溶解度会减小.
解答 解:A、在加热氯酸钾和二氧化锰的反应中,二氧化锰是反应的催化剂,本身质量不变,氯酸钾分解生成氯化钾和氧气,固体质量减少,所以二氧化锰的质量分数增大,故A正确;
B、向盐酸中加入水,则盐酸被稀释,酸性减弱,pH增大,但是不会大于等于7,故B正确;
C、氢氧化钠能与硫酸铜反应生成氢氧化铜沉淀,氢氧化钠和氢氧化铜都会与硫酸反应,故反应开始时不能形成氢氧化铜沉淀,即氢氧化钠先与硫酸反应,等盐酸消耗尽,氢氧化钠与硫酸铜反应生成氢氧化铜沉淀,故C正确;
D、加热蒸发稀盐酸,溶质氯化氢的溶质质量分数会减小,故溶质会减少,不会是溶质质量分数增大,故D错误;
故选D.
点评 本题考查了反应过程中的有关图象问题,完成此题,可以依据已有的知识结合具体的反应进行.

练习册系列答案
相关题目
4.如图所示的实验操作,正确的是( )
| A. | 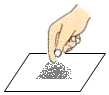 取用固体 | B. | 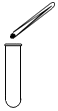 \ \加入块状固体 | C. | 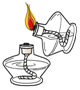 点燃酒精灯 | D. | 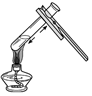 加热液体 |
17.某化学兴趣小组围绕“酸和碱的中和反应”的学习,进行了如下实验.
实验一:5mL氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,可观察到现象为溶液变红,然后加入稀盐酸,用玻璃棒搅拌,溶液褪为无色,有关的反应方程式为HCl+NaOH═NaCl+H2O.
实验二:对实验一反应后溶液中的溶质进行探究.
【提出猜想】
猜想一:只有NaCl
猜想二:有NaCl和NaOH
猜想三:有NaCl和HCl
你认为猜想二不合理,其理由是此时溶液呈无色,而氢氧化钠能使酚酞试液变红.
【设计实验】
【拓展应用】我国土壤的酸碱性有“南酸北碱”之说法,你认为需向酸性土壤中加入熟石灰进行改良.
实验一:5mL氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,可观察到现象为溶液变红,然后加入稀盐酸,用玻璃棒搅拌,溶液褪为无色,有关的反应方程式为HCl+NaOH═NaCl+H2O.
实验二:对实验一反应后溶液中的溶质进行探究.
【提出猜想】
猜想一:只有NaCl
猜想二:有NaCl和NaOH
猜想三:有NaCl和HCl
你认为猜想二不合理,其理由是此时溶液呈无色,而氢氧化钠能使酚酞试液变红.
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入石蕊试液 | 溶液变红 | 猜想三成立 |
1.如图所示实验操作中,错误的是( )
| A. | 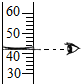 量取液体 | B. | 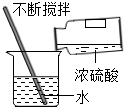 浓硫酸稀释 浓硫酸稀释 | C. |  CO2的验满 | D. | 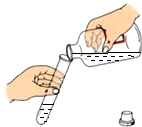 液体的倾倒 |
11.下列变化中,属于化学变化的是( )
| A. | 水制冰块 | B. | 菠萝榨汁 | C. | 食物腐烂 | D. | 氧气易溶于水中 |
16.下列试剂中,能区别氢氧化钠溶液和澄清石灰水的是( )
| A. | 二氧化碳 | B. | 石蕊溶液 | C. | 稀盐酸 | D. | 酚酞溶液 |
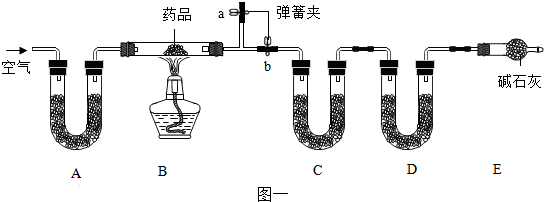

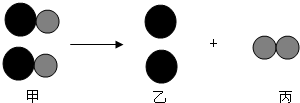
 ”和“
”和“ ”分别表示不同质子数的原子在化学变化前后的微观模拟示意图下.请回答下列问题:
”分别表示不同质子数的原子在化学变化前后的微观模拟示意图下.请回答下列问题: