题目内容
5.某溶液中大量存在的离子仅有Ca2+、NH4+和X离子,则X可能是BA.CO32-B.NO3-C.OH-D.Cl-.
分析 根据离子之间不能结合生成沉淀、气体、水、弱电解质,则离子能大量共存,以此来解答.
解答 解:某溶液中大量存在的离子仅有Ca2+、NH4+和X离子,所以X离子必须与Ca2+、NH4+能够共存,相互结合不能产生沉淀、气体和水.
A、CO32-与Ca2+结合产生碳酸钙沉淀,故A错;
B、NO3-能与Ca2+、NH4+共存,故B正确;
C、OH-与NH4+结合产生氨气和水,所以不能共存,故C错;
D、Cl-能与Ca2+、NH4+共存.
故答案为:B;Cl-
点评 本题考查离子的共存,熟悉离子之间的反应即可解答,题目难度不大.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
16.下列物质的用途中,利用其化学性质的是( )
| A. | 干冰用于人工降雨 | B. | 石墨可用作电极 | ||
| C. | 用已烷提取大豆油 | D. | 氢能源用于汽车 |
13.水是生命之源,下列有关水的说法错误的是( )
| A. | 自来水是通过沉淀、过滤、蒸馏等操作制得的 | |
| B. | 日常生活中,居民通过加热煮沸可以降低水的硬度 | |
| C. | 可用肥皂水区分硬水和软水 | |
| D. | 用活性炭净水时没有除去水中的微生物、矿物质 |
20.下列相关事实用微观粒子的知识解释错误的是 ( )
| 选项 | 事 实 | 解 释 |
| A | 端午时节粽飘香 | 分子不断运动 |
| B | 酒精溶液是混合物 | 由不同种分子构成 |
| C | 水加热变成水蒸气,体积变大 | 水分子之间的间隙变大 |
| D | 蔗糖水中的蔗糖晶体受热消失 | 蔗糖分子受热分解了 |
| A. | A | B. | B | C. | C | D. | D |
14.醋的主要成分是醋酸,其化学式为CH3COOH,醋不仅是调味品,而且还有较强的灭菌、抑毒的作用.

小明为判断家中的米醋含酸量是否合格,取100mL米醋(见标签)于锥形瓶中,然后再向锥形瓶中逐渐加入一定溶质质量分数的碳酸氢钠溶液,反应过程中,当加入碳酸氢钠溶液的质量至以下数值时,对充分反应后锥形瓶中剩余物质的质量进行了记录,测得的部分数据如下,请根据有关信息回答问题(提示:化学方程式为:CH3COOH+NaHCO3═CH3COONa+H2O+CO2↑)
(1)醋酸中碳、氢、氧三种元素的质量比为6:1:8.
(2)100mL米醋与足量碳酸氢钠溶液反应产生的二氧化碳质量为6.6g,表中m的数值为268.4.
(3)请通过计算判断该产品含酸量是否合格?(写出计算过程)

小明为判断家中的米醋含酸量是否合格,取100mL米醋(见标签)于锥形瓶中,然后再向锥形瓶中逐渐加入一定溶质质量分数的碳酸氢钠溶液,反应过程中,当加入碳酸氢钠溶液的质量至以下数值时,对充分反应后锥形瓶中剩余物质的质量进行了记录,测得的部分数据如下,请根据有关信息回答问题(提示:化学方程式为:CH3COOH+NaHCO3═CH3COONa+H2O+CO2↑)
| 加入碳酸氢钠溶液质量(g) | 25 | 50 | 100 | 155 | 175 |
| 锥形瓶内剩余物质质量(g) | 123.9 | 147.8 | 195.6 | 248.4 | m |
(2)100mL米醋与足量碳酸氢钠溶液反应产生的二氧化碳质量为6.6g,表中m的数值为268.4.
(3)请通过计算判断该产品含酸量是否合格?(写出计算过程)
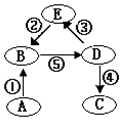 已知A、B、C、D、E五种物质中都含有人体含量最多的一种金属元素,其中A是单质,B、C都是含有两种元素的化合物,D、E都是含有三种元素的化合物,反应⑤是放热反应,它们之间的转化关系如图所示.请回答:
已知A、B、C、D、E五种物质中都含有人体含量最多的一种金属元素,其中A是单质,B、C都是含有两种元素的化合物,D、E都是含有三种元素的化合物,反应⑤是放热反应,它们之间的转化关系如图所示.请回答: