题目内容
15.黄铜(锌和铜的合金)、生铁是两种常见的合金.(1)将黄铜放入足量的稀盐酸中,现象是有大量气泡产生,发生反应的化学方程式是Zn+2HCl═ZnCl2+H2↑,最后残留的固体是铜.
(2)将生铁放入足量的稀盐酸中,反应的方程式是Fe+2HCl═FeCl2+H2↑,所属基本反应类型是置换反应,最后残留的固体主要是碳.
分析 (1)黄铜是锌和铜的合金,锌的金属活动性比氢强,铜的金属活动性比氢弱,锌能与稀盐酸反应,铜不能与稀盐酸反应,据此进行分析解答.
(2)生铁的主要成分是铁,含有碳等杂质,铁的金属活动性比氢强,碳不能与稀盐酸反应,据此进行分析解答.
解答 解:(1)黄铜是锌和铜的合金,锌的金属活动性比氢强,铜的金属活动性比氢弱,锌能与稀盐酸反应,铜不能与稀盐酸反应,将黄铜放入足量的稀盐酸中,现象是有大量气泡产生;锌与稀盐酸反应生成氯化锌和氢气,反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑;最后残留的固体是铜.
(2)生铁的主要成分是铁,含有碳等杂质,铁的金属活动性比氢强,碳不能与稀盐酸反应,将生铁放入足量的稀盐酸中,铁与稀盐酸反应生成氯化亚铁和氢气,反应的方程式是Fe+2HCl═FeCl2+H2↑;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应;最后残留的固体主要是碳.
故答案为:(1)有大量气泡产生;Zn+2HCl═ZnCl2+H2↑;铜;
(2)Fe+2HCl═FeCl2+H2↑;置换反应;碳.
点评 本题难度不大,掌握金属的化学性质、生铁的主要成分、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
20.下列各组物质的溶液,不用另加试剂就可以鉴别出来的是(不可加热,且用化学方法)( )
| A. | Na2SO4 BaCl2 NaNO3 KNO3 | B. | CuSO4 NaOH NaNO3 KCl | ||
| C. | NaCl AgNO3 HCl NaNO3 | D. | K2CO3 K2SO4 H2SO4 Ba(NO3)2 |
10.下列表示“CH4”的含义不正确的是( )
| A. | 表示甲烷这种物质 | |
| B. | 表示甲烷由碳氢两种元素组成 | |
| C. | 表示甲烷由1个碳原子和4个氢原子构成 | |
| D. | 表示一个甲烷分子 |
11.下列实验操作中,错误的是( )
| A. |  滴加液体 | B. |  加热液体 | C. |  稀释浓硫酸 | D. |  检查气密性 |
 通过化学学习,同学们对组成万物的基本物质有了进一步了解.
通过化学学习,同学们对组成万物的基本物质有了进一步了解. ,则X=11.
,则X=11.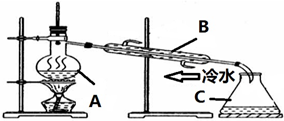 如图所示是从硬水中制取蒸馏水的装置.
如图所示是从硬水中制取蒸馏水的装置.