题目内容
6.分析五种物质:Fe、Fe2O3、NaOH溶液、AgNO3溶液、稀盐酸,回答问题:(1)五种物质中有一种物质能与其他四种物质发生反应,该物质是稀盐酸;
(2)能与稀盐酸反应应具有盐和水生成的物质有Fe2O3、NaOH;
(3)要通过一步反应来制取氯化铁溶液,可选择上述物质中的Fe2O3、稀盐酸;
(4)将其中的两种溶液混合后有白色沉淀产生,该反应可用化学方程式表示为HCl+AgNO3 =HNO3 +AgCl↓.
分析 (1)根据酸的性质进行解答;
(2)根据氧化铁和盐酸反应生成氯化铁和水,氢氧化钠和盐酸反应生成氯化钠和水进行解答;
(3)根据氧化铁和盐酸反应生成氯化铁和水进行解答;
(4)根据盐酸和硝酸银反应生成氯化银沉淀和硝酸进行解答.
解答 解:(1)酸的化学性质能与活泼金属、金属氧化物、碱、碳酸盐等反应,所以盐酸能和Fe、Fe2O3、NaOH溶液、AgNO3溶液反应;故填:稀盐酸;
(2)氧化铁和盐酸反应生成氯化铁和水,氢氧化钠和盐酸反应生成氯化钠和水,所以能与稀盐酸反应应具有盐和水生成的物质有氧化铁和氢氧化钠;故填:Fe2O3、NaOH;
(3)氧化铁和盐酸反应生成氯化铁和水;故填:Fe2O3、稀盐酸;
(4)盐酸和硝酸银反应生成氯化银沉淀和硝酸,化学方程式为HCl+AgNO3 =HNO3 +AgCl↓.故填:HCl+AgNO3 =HNO3 +AgCl↓.
点评 本题难度不大,掌握酸的化学性质(能与活泼金属、金属氧化物、碱、碳酸盐等反应)并能灵活运用是正确解答本题的关键.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
16.下列实验操作正确的是( )
| A. |  检验溶液酸碱性 | B. |  溶解固体 | C. | 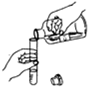 倾倒液体 | D. | 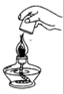 熄灭酒精灯 |
17.下列气体中既可以用浓硫酸干燥,又可以用固体氢氧化钠干燥的是( )
| A. | O2 | B. | NH3 | C. | SO2 | D. | CO2 |
1.下列属于纯净物的是( )
| A. | 稀盐酸 | B. | 干冰 | C. | 大理石 | D. | 钢 |