题目内容
17.指出下列符号中“2”的含义:(1)2Hg汞原子的个数为2;(2)O21个氧分子中含有2个氧原子;(3)2Fe2+系数2亚铁离子的个数为2;“2+”一个亚铁离子带有两个单位的正电荷;(4)$\stackrel{+2}{Mg}$O氧化镁中镁元素的化合价为+2价.
分析 (1)标在元素符号前面的数字表示原子的个数.
(2)标在化学式中元素右下角的数字表示一个分子中所含原子的数目.
(3)标在离子符号前面的数字表示离子的个数,标在元素符号右上角的数字表示离子所带电荷数.
(4)标在元素符号正上方的数字表示该元素化合价的数值.
解答 解:(1)标在元素符号前面的数字表示原子的个数,2Hg中的“2”表示汞原子的个数为2.
(2)标在化学式中元素右下角的数字表示一个分子中所含原子的数目,O2中的“2”表示1个氧分子中含有2个氧原子.
(3)标在离子符号前面的数字表示离子的个数,2Fe2+中的系数“2”表示亚铁离子的个数为2;标在元素符号右上角的数字表示离子所带电荷数,Fe2+中的“2+”表示一个亚铁离子带有两个单位的正电荷.
(4)标在元素符号正上方的数字表示该元素化合价的数值,$\stackrel{+2}{Mg}$O可表示氧化镁中镁元素的化合价为+2价.
故答案为:(1)汞原子的个数为2;(2)1个氧分子中含有2个氧原子;(3)亚铁离子的个数为2;一个亚铁离子带有两个单位的正电荷;(4)氧化镁中镁元素的化合价为+2价.
点评 本题难度不大,主要考查了元素符号不同位置的数字表示的意义,掌握标在元素符号不同位置的数字所表示的意义是正确解答此类题的关键所在.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.新泰天宝是樱桃之乡.樱桃中富含的中富含的维生素A1;具有预防夜盲症、抗衰老和促进骨骼生长等功效,其化学式为C20H30O.下列说法正确的是( )
| A. | 维生素A1的相对分子质量为286g | |
| B. | 维生素A1分子由碳元素、氢元素和氧元素组成 | |
| C. | 维生素A1中碳元素的质量分数最大 | |
| D. | 维生素A1由20个碳原子、30个氢原子、1个氧原子构成 |
6.碳元素与氧元素最本质的区别是( )
| A. | 相对原子质量不同 | B. | 质子数不同 | ||
| C. | 电子数不同 | D. | 中子数不同 |
12.在原子中,质子数等于( )
| A. | 中子数 | B. | 核外电子数 | C. | 电子层数 | D. | 最外层电子数 |
4.“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一,请回答下列问题:
(1)某同学用托盘天平称取氯化钠固体19g,用量筒量取蒸馏水76mL(水的密度为1g/cm3),配制一定溶质质量分数的氯化钠溶液,该氯化钠溶液的溶质质量分数为20%;
下列实验操作与目的分析均正确的一组是D(填字母序号).
(2)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,此时需要用到的玻璃仪器有:烧杯、玻璃棒、量筒和胶头滴管;若量取水时俯视读数,则所配制的氯化钠溶液溶质质量分数会偏大(填“偏大”、“不变”、“偏小”).
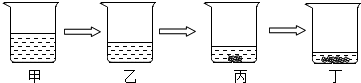
(3)实验室若用恒温蒸发的方法将15%的氯化钠溶液变成饱和溶液,其过程如图所示.与丙烧杯中溶液溶质质量分数一定相同的是丁烧杯中的溶液.
(1)某同学用托盘天平称取氯化钠固体19g,用量筒量取蒸馏水76mL(水的密度为1g/cm3),配制一定溶质质量分数的氯化钠溶液,该氯化钠溶液的溶质质量分数为20%;
下列实验操作与目的分析均正确的一组是D(填字母序号).
| 项目 | 实验操作 | 目的分析 |
| A | 称取氯化钠时,将取出的过量氯化钠放回原瓶 | 节约药品 |
| B | 溶解氯化钠时用玻璃棒搅拌 | 增强氯化钠的溶解能力 |
| C | 称取氯化钠时,在天平两边托盘上各放一张质量相等的纸 | 整洁美观 |
| D | 最取所需水时,视线与量筒内液体凹液面的最低处保持水平 | 准确读数 |
(3)实验室若用恒温蒸发的方法将15%的氯化钠溶液变成饱和溶液,其过程如图所示.与丙烧杯中溶液溶质质量分数一定相同的是丁烧杯中的溶液.

