题目内容
“过碳酸钠”(2Na2CO3·3H2O2)俗称固体双氧水,它既有碳酸盐的性质,又有双氧水的不稳定性和氧化性,是很好的消毒剂和供氧剂,广泛应用于洗涤、印染和医药等领域.“过碳酸钠”的制备流程如下:
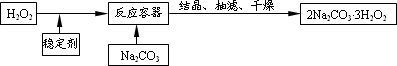
请回答下列问题:
(1)H2O2在催化或受热条件下易分解,其化学方程式为________;在上述流程中,向反应前的H2O2中加入稳定剂的作用是________.
(2)在“过碳酸钠”中加入下列物质时,不会导致“过碳酸钠”变质的是________(填序号).
A.二氧化锰
B.稀盐酸
C.硫酸钠
D.石灰水
(3)“过碳酸钠”极易分解,得到碳酸钠、水和氧气,其反应方程式可表示为
2(2Na2CO3·3H2O2)请通过计算说明:①若“过碳酸钠”分解产生氧气12 g,则同时产生碳酸钠的质量是多少?
②若将上述产生的碳酸钠全部配制成溶质质量分数为10.6%的溶液,需加水的质量是多少?
答案:⑴ 2H2O2 =2H2O+ O2↑ ;防止双氧水分解
⑵C
⑶ 生成Na2CO3的质量为53g,配成10.6%的溶液需加水的质量为447g。
⑵C
⑶ 生成Na2CO3的质量为53g,配成10.6%的溶液需加水的质量为447g。

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目

