题目内容
3.酸、碱、盐都是重要的化合物.请回答下列有关问题: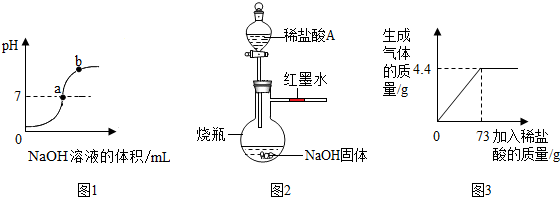
(1)酸和碱能发生中和反应,其水溶液都能使酸碱指示剂变色.请再写一条酸碱在组成或性质方面的共同点:组成上都含有氢元素;性质上都可以和某些盐或氧化物反应.
(2)固体MgH2是氢能源汽车的供能剂,MgH2可以和水反应生成一种碱,同时释放出氢气,该反应的化学方程式是MgH2+2H2O=Mg(OH)2+2H2↑.
(3)如图1是利用数字化传感器得到的盐酸和氢氧化钠反应溶液pH变化图象.图中b点所示溶液中,含有的溶质是NaCl NaOH.
(4)为了探究酸碱中和反应中是否放热,某同学设计了如图2所示的实验装置.
①请你分析这个实验的不足之处并加以改进?
②改进后,观察到的什么现象说明中和反应放热?
(5)某品牌纯碱中含杂质NaCl,小明同学进行了如下实验探究:称取12g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图3.纯碱恰好完全反应时,生成CO2的质量为4.4g?该样品中含杂质的质量分数是多少?(精确到0.1%)
分析 (1)根据由酸碱的性质可知,酸和碱在组成上都含氢元素,在性质上强酸强碱都有腐蚀性解答;
(2)根据化学反应前后,元素的种类不变,原子的种类、总个数不变解答;
(3)根据b点时,pH>7,溶液显碱性,氢氧化钠过量解答;
(4)
①氢氧化钠溶于水也会放出热量,所以不能用氢氧化钠固体来进行实验,应该选择氢氧化钠的浓溶液来进行实验,可以据此解答该题;
②反应若放出热量,则会使烧瓶中的气体受热而膨胀,从而将红墨水向右推移,可以据此解答.
(5)由图示可知生成的二氧化碳的质量;根据化学方程式由二氧化碳的质量可以求出碳酸钠的质量和生成的氯化钠的质量,进而可以求出杂质的质量及质量分数;
解答 解:
(1)由酸碱的性质可知,酸和碱在组成上都含氢元素,在性质上强酸强碱都有腐蚀性;
(2)MgH2可以和水反应生成氢氧化镁和氢气,该反应的化学方程式为:MgH2+2H2O═Mg(OH)2+2H2↑.
(3))b点时,pH>7,溶液显碱性,氢氧化钠过量,含有的溶质是NaOH和NaCl.
(4)
①氢氧化钠溶于水也会放出热量,所以不能用氢氧化钠固体来进行实验,应该选择氢氧化钠的浓溶液来替换氢氧化钠固体来进行实验;
②反应若放出热量,则会使烧瓶中的气体受热而膨胀,从而将红墨水向右推移,所以若观察到红墨水右移,则说明中和反应放热.
(5)由图示可知生成的二氧化碳的质量为4.4g;
设样品中含碳酸钠的质量为x,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$
x=10.6g
样品中含杂质的质量分数为:$\frac{12g-10.6g}{12g}$×100%≈11.7%
答案:
(1)组成上都含有氢元素;性质上都可以和某些盐或氧化物反应
(2)MgH2+2H2O=Mg(OH)2+2H2↑
(3)NaCl NaOH
(4)
①氢氧化钠固体溶于水也会放出大量的热,应用氢氧化钠的浓溶液来代替氢氧化钠固体
②若观察到红墨水右移,则说明中和反应放热.
(5)4.4 该样品中含杂质的质量分数是11.7%
点评 要想解答好这类题目,首先,要理解和熟记中和反应及其应用等相关知识.然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

 轻松暑假总复习系列答案
轻松暑假总复习系列答案| A. | 水、空气、煤都是混合物 | B. | 石墨、盐水、铅、人体是导体 | ||
| C. | 沥青、食盐、铁、冰都是晶体 | D. | 硝酸钾、氯化钾、磷酸钾都是钾肥 |
| A. | 氧化铁加入稀盐酸中 | B. | 二氧化碳通入足量石灰水中 | ||
| C. | 氢氧化钠溶液和稀盐酸混合 | D. | 碳酸氢钠粉末加入稀盐酸中 |
| A. | 火碱 | B. | 烧碱 | C. | 熟石灰 | D. | 小苏打 |
| A. | Zn、Na、Ag | B. | Zn、Ag | C. | Na、Ag | D. | Ag |
| A、实验方法 | B、化学与生活 |
| ①鉴别O2、CO2--可用澄清石灰水 ②熄灭酒精灯--用灯帽盖灭 ③除去水瓶中的水垢--用稀盐酸 | ①人体缺铁会引起贫血症 ②进入久未开启的菜窖时先做灯火实验 ③用活性炭净水器可净化水 |
| C、实验记录 | D、物质构成 |
| ①用10mL量筒量取8mL水 ②滴有紫色石蕊试液的水中通入CO2后 变红 ③用托盘天平称取5.6g食盐 | ①分子、原子、离子都是构成物质的微粒 ②空气、液氧、二氧化硫中都含有氧分子 ③碳酸钠的化学式为 NaCO3 |
| A. | A | B. | B | C. | C | D. | D |
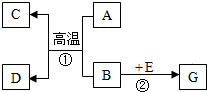 A~H是初中化学常见的物质,它们之间的相互关系如图所示,其中A是黑色粉末、B是红棕色粉末(一种铁矿石主要成分),C常温下为气体,G是一种盐.请回答下面问题:
A~H是初中化学常见的物质,它们之间的相互关系如图所示,其中A是黑色粉末、B是红棕色粉末(一种铁矿石主要成分),C常温下为气体,G是一种盐.请回答下面问题: