题目内容
4.如图为某化工企业生产流程示意图,下列说法正确的是( )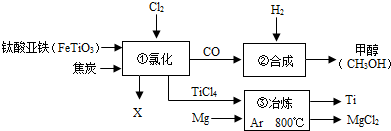
| A. | ③中氩气(Ar)作反应物 | |
| B. | 钛酸亚铁是铁和钛的合金 | |
| C. | ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1 | |
| D. | ①中反应为:2FeTiO3+6C+7Cl2$\frac{\underline{\;一定条件\;}}{\;}$2X+2TiCl4+6CO,则X为FeCl2 |
分析 A.根据氩气的化学性质来分析;
B.根据合金的概念考虑;
C.根据氢气和一氧化碳反应的方程式考虑质量比;
D.根据化学反应前后,原子的种类和数目均不改变来分析.
解答 解:A.氩气是一种稀有气体,化学性质稳定,在反应过程中作保护气,故错误;
B.钛酸亚铁是由铁、钛、氧三种元素组成的化合物,不是合金,故错误;
C.根据从化学方程式2H2+CO═CH3OH
4 28
由此可知一氧化碳和氢气的质量比是:28:4=7:1,故正确;
D.根据质量守恒定律,在反应前后各元素原子的个数不变.从2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO看钛原子、氧原子、碳原子反应前后除物质x外个数已经相等,故x中无钛原子、氧原子、碳原子.铁反应前共有2个,反应后只有x有,所以2x中有2个,从而x中有1个;氯原子反应前有14个,反应后x除外有8个,所以2x中有6个,因此x中有3个,因此x的化学式是FeCl3,故错误.
故选C.
点评 本题主要考查了化学方程式的书写以及质量守恒定律的应用,同时考查了学生从题目中获取信息并运用的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.除去CO2中混有的CO(少量),应采用的正确方法是( )
| A. | 将气体通入浓硫酸中 | B. | 将气体通入石灰水中 | ||
| C. | 将气体通过赤热的氧化铜 | D. | 将气体通过赤热的碳 |
12.食品卫生与身体健康是密切相关的.下列做法会导致食品对人体健康有害的是( )
| A. | 用石灰水保存新鲜鸡蛋 | B. | 食品中添加过量防腐剂 | ||
| C. | 蒸馒头加入适量纯碱 | D. | 在食盐中适量添加碘元素 |
19.下列物质属于纯净物的是( )
| A. | 医用酒精 | B. | 冰水 | C. | 清新空气 | D. | 加碘食盐 |
16.agH2O2溶液与bgMnO2,完全反应后,剩余物的质量为cg,则反应产生氧气质量( )
| A. | (a+b-c)g | B. | (a-c)g | C. | (a-b-c)g | D. | (a+b)g |