题目内容
13.通过化学学习,应该知道有多种途径制取氧气.如:a、加热氯酸钾晶体和二氧化锰粉末;b、加热高锰酸钾;c、用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气;d、分离空气等.如图是实验室常见的制取气体的装置:

(1)请填写b处另一种制取氧气的方法加热高锰酸钾.
(2)请仔细分析装置A的特点,推测其所用的制氧气的方法是a(填a、b、c或d).装置A中发生反应的文字表达式:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气,该反应基本类型是分解反应.
(3)采用方法c制取氧气应选择的发生装置是B,锥形瓶中应先放入的药品是二氧化锰,方法c发生反应的文字表达式:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,其中锥形瓶放入药品起催化作用,它与采用装置A制取氧气相比较,主要优点是不加热,操作简便等(任答一条).
(4)若用排水法收集氧气时,当观察到气泡连续、均匀地放出时才开始收集,否则收集的氧气不纯.某同学收集完毕,先停止加热再将导管移出水面,你预测这种操作可能会引起的后果是炸裂试管.如果选用装置D收集氧气,收集氧气的依据是氧气密度比空气大,检验装置D中氧气是否收集满的方法:将带火星的木条伸到集气瓶口,若木条复燃,证明氧气已收满.
(5)通过查阅资料得知:硫化氢(H2S)是一种有毒气体,其密度比空气大,且能溶于水,水溶液呈酸性.实验室通常用硫化亚铁(固体)与稀硫酸(液体)在常温下通过复分解反应制得.小芳同学在实验室制取硫化氢气体,她应选择反应的发生装置是B(填序号,下同),收集装置是D.
分析 (1)根据制取氧气的方法来分析;
(2)根据实验装置确定制取原理,书写文字表达式以及判断反应的类型;
(3)根据反应的原理确定制取原理、结合装置的特点分析解答;
(4)根据氧气的收集方法以及操作中的注意事项和验满方法来分析;
(5)根据实验室制取硫化氢的反应物状态、反应条件、硫化氢的性质可以选择发生装置和收集装置.
解答 解:(1)在实验室中可以用加热高锰酸钾的方法制取氧气;故填:加热高锰酸钾;
(2)装置A属于固体加热制取氧气,试管口没有棉花团,所以是加热氯酸钾和二氧化锰的混合物制取氧气,同时生成氯化钾;该反应符合“一变多”的特征,属于分解反应;故填:a;氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;分解;
(3)方法c是固液常温下制取氧气,所以是过氧化氢在二氧化锰的催化作用下生成水和氧气,故选择装置B;锥形瓶内加入的是固体药品二氧化锰,二氧化锰是催化剂,加快了过氧化氢的分解速率,此方法制取氧气无需加热、操作方便;故填:B;二氧化锰;过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;催化;不加热,操作简便等;
(4)用排水法收集氧气时,导管口开始冒出的是装置内的空气,不能收集,应该等到气泡连续而且均匀冒出时才能收集;结束实验时要先撤离导管出水面,再熄灭酒精灯,其目的是防止水倒吸入热的试管,引起试管炸裂;氧气的密度比空气大,所以可用向上排空气法来收集,检验氧气是否收集满可利用氧气支持燃烧的性质,利用带火星的木条放于集气瓶口,观察木条是否复燃,确定是否收集满;故填:连续、均匀地放出;炸裂试管;氧气密度比空气大;将带火星的木条伸到集气瓶口,若木条复燃,证明氧气已收满;
(5)实验室用硫化亚铁与稀硫酸反应制取硫化氢气体时不需要加热,应该用B装置作为发生装置;硫化氢能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用D装置收集.故填:B、D.
点评 本题主要考查氧气的制法、化学方程式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、密度、能否和空气中的物质发生化学反应等因素.

| A. | 木炭在空气中燃烧后,生成黑色的固体 | |
| B. | 硫粉在氧气中燃烧,产生紫色火焰 | |
| C. | 镁条在空气中燃烧,耀眼的白色火焰 | |
| D. | 红磷在空气中燃烧,产生蓝紫色火焰 |
| A. | 水 | B. | 澄清石灰水 | C. | 食盐水 | D. | 糖水 |
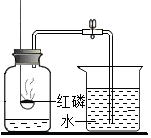 如图所示是测定空气中氧气含量的实验装置,试回答下列问题.
如图所示是测定空气中氧气含量的实验装置,试回答下列问题.