题目内容
4.镁及其化合物在生产、生活中应用广泛.(1)从海水中提取金属镁,可按如图所示流程进行:

①下列说法正确的是B(填字母).
A.步骤Ⅰ通过一步反应即可实现 B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁
C.步骤Ⅴ中化学能转化为电能 D.该流程涉及的基本反应类型有4种
②该流程中采取的一种降低成本且减少污染的措施是将氯化氢循环利用.
分析 步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁,其中牵扯的化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;CaO+H2O=Ca(OH)2;Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2;2HCl+Mg(OH)2═MgCl2+2H2O;化合反应的特点“多变一”;分解反应的特点“一变多”;复分解反应的特点是两种化合物相互交换成分,生成另外两种化合物;置换反应的特点是单质和化合物生成单质和化合物,由此可知该过程无置换反应.
解答 解:①A、CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;CaO+H2O=Ca(OH)2步骤Ⅰ通过两步反应即可实现;
B、步骤Ⅱ、Ⅲ可得到氢氧化镁沉淀,步骤Ⅳ加入盐酸,可得到氯化镁,故B正确;
C、步骤Ⅴ中化学能转化为电能,说法错误,应为电能转化为化学能;
D、在此流程中涉及的基本反应类型有3种,无置换反应.
故选B.
②生成的氯化氢气体溶于水形成盐酸还可以和氢氧化镁反应,所以在此流程中可以循环利用的物质是氯化氢;故填:将氯化氢循环利用.
点评 本题以海洋资源的开发和利用为研究性学习的课题,视角新颖,中考题目以这种方式出现,以化学学科知识结合生活、生产、社会问题展开.

练习册系列答案
相关题目
15.下列有关溶解度的说法,正确的是( )
| A. | 20℃时,100克水里溶解了20克某物质,则在20℃时,该物质的溶解度为20克 | |
| B. | 100克水中溶解40克物质刚好饱和,则该物质的溶解度为40克 | |
| C. | 50℃时,50克水中最多可溶解20克某物质,则100℃时该物质的溶解度为20克 | |
| D. | 20℃时,30克某物质中逐渐加入水,当加入100克水时,该物质恰好完全溶解,则20℃时该物质的溶解度为30克 |
19. 钒被誉为“合金的维生素”,钒元素的相关信息如图,下列有关钒的说法正确的是( )
钒被誉为“合金的维生素”,钒元素的相关信息如图,下列有关钒的说法正确的是( )
 钒被誉为“合金的维生素”,钒元素的相关信息如图,下列有关钒的说法正确的是( )
钒被誉为“合金的维生素”,钒元素的相关信息如图,下列有关钒的说法正确的是( )| A. | 属于非金属元素 | B. | 原子核内中子数为23 | ||
| C. | 原子核外电子数为23 | D. | 相对原子质量为50.94g |
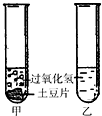 小明将一片土豆放入过氧化氢溶液中,发现过氧化氢溶液的分解速率加快.查阅资料后知道土豆中含有一种生物催化剂--过氧化氢酶,于是他设计了如下实验:常温下将几片土豆放入甲试管,分别往甲、乙试管内注入相同体积与溶质质量分数的过氧化氢溶液(如图所示),观察试管内气泡产生的速率.
小明将一片土豆放入过氧化氢溶液中,发现过氧化氢溶液的分解速率加快.查阅资料后知道土豆中含有一种生物催化剂--过氧化氢酶,于是他设计了如下实验:常温下将几片土豆放入甲试管,分别往甲、乙试管内注入相同体积与溶质质量分数的过氧化氢溶液(如图所示),观察试管内气泡产生的速率.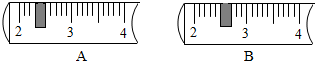 阳阳家有一个奶牛养殖场,一天奶牛得了急性肠炎,通过询问兽医他知道了用0.1%的高锰酸钾溶液冲洗肠胃可以辅助治疗.阳阳家一共需要0.1%的高锰酸钾溶液2500g,他决定帮妈妈配制所需的高锰酸钾溶液.
阳阳家有一个奶牛养殖场,一天奶牛得了急性肠炎,通过询问兽医他知道了用0.1%的高锰酸钾溶液冲洗肠胃可以辅助治疗.阳阳家一共需要0.1%的高锰酸钾溶液2500g,他决定帮妈妈配制所需的高锰酸钾溶液.