题目内容
19.食醋是一种常用的调味剂,其主要成分为醋酸(CH3COOH也常写成HAc),是种一元弱酸,食醋除作为调味剂外,还有其它的用途,如在流感流行时作为熏蒸剂消毒;也可代替盐酸用于浸泡除去热水瓶内胆壁上的水垢(水垢的主要成分是碳酸钙,假设食醋中的其它成分不和碳酸钙反应)浸泡过程中有CO2产生,这说明醋酸的酸性比碳酸强(填“强”或“弱”或“相等”);醋酸的水溶液可以导电,说明醋酸是电解质;往醋酸溶液或盐酸溶液中滴入石蕊指示剂,石蕊指示剂会变红,而滴入醋酸钠溶液(NaAc)或NaCl溶液中,石蕊指示剂不会变红,说明使石蕊指示剂变红的是因为溶液中存在较多的H+(填“H+”或“Na+”或“Ac-”或“Cl-”)分析 根据题意,食醋的主要成分为醋酸,可代替盐酸用于浸泡除去热水瓶内胆壁上的水垢(水垢的主要成分是碳酸钙),电解质的水溶液能够导电,结合石蕊溶液遇酸性溶液变红色,进行分析解答.
解答 解:食醋的主要成分为醋酸,可代替盐酸用于浸泡除去热水瓶内胆壁上的水垢(水垢的主要成分是碳酸钙),即醋酸能与碳酸钙反应生成二氧化碳气体,则说明醋酸的酸性比碳酸强.
醋酸的水溶液可以导电,说明醋酸中含有能自由运动的离子,是电解质.
往醋酸溶液或盐酸溶液中滴入石蕊指示剂,石蕊指示剂会变红,而滴入醋酸钠溶液(NaAc)或NaCl溶液中,石蕊指示剂不会变红,醋酸溶液或盐酸溶液中含有氢离子、“Ac-”或“Cl-”,而醋酸钠溶液(NaAc)或NaCl溶液中含有钠离子、“Ac-”或“Cl-”,则说明使石蕊指示剂变红的是因为溶液中存在较多的H+.
故答案为:强;电解质;H+.
点评 本题难度不大,掌握酸的化学性质并能灵活运用是正确解答本题的关键.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
10.下列变化属于化学变化的是( )
| A. | 石蜡熔化 | B. | 酒精挥发 | C. | 粮食酿酒 | D. | 干冰升华 |
14.目前有部分学生在做作业或考试时,喜欢使用修正液(涂改液),经实验证明,修正液中含有多种挥发性有害物质,吸入后易引起头晕、头痛,严重者会呼吸困难、抽搐.三氯乙烷(CH3CCl3)就是其中的一种.下面关于三氯乙烷的几种叙述正确的是( )
| A. | 是碳、氢、氯三种元素组成的化合物 | |
| B. | 它的分子中碳、氢、氯元素的原子个数比为1:3:3 | |
| C. | 它的式量为CH4的6倍 | |
| D. | 它是冰箱中常用的制冷剂 |
4.下列说法中,正确的是( )
| A. | 含冰的水是混合物 | |
| B. | 原子由质子和中子组成 | |
| C. | 在物质HRO4中,R元素的化合价为+7价 | |
| D. | 相同分子数目的氧气分子和氢气分子的质量比为32:1 |
18.在加热条件下,汞和氧气能发生反应,其反应的微观示意图如图,下列说法正确的是( )
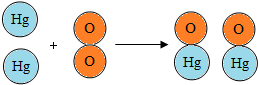

| A. | 所有化学反应在反应前后原子个数都不发生变化 | |
| B. | 汞是由分子构成的 | |
| C. | 该反应属于复分解反应 | |
| D. | 由微观示意图可知:参加的汞和氧气的质量比为2:1 |
 如图是某同学设计的制取二氧化碳并将二氧化碳通入紫色石蕊试液的装置图,回答下列有关问题.
如图是某同学设计的制取二氧化碳并将二氧化碳通入紫色石蕊试液的装置图,回答下列有关问题.