题目内容
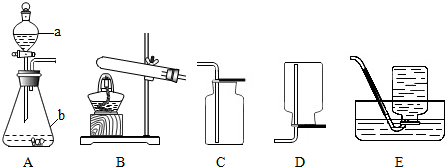
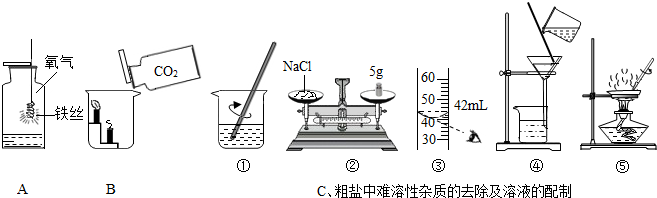
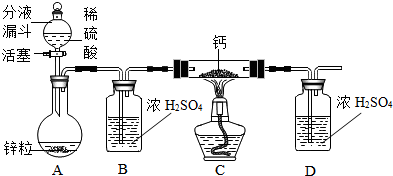
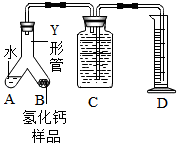
某校的化学学习小组根据下面给出的药品和实验装置,设计一个实验,粗略测定由铜和锌两种金属组成的合金-黄铜中锌的质量分数(黄铜已加工成粉末).实验装置如图(另有托盘天平可用):
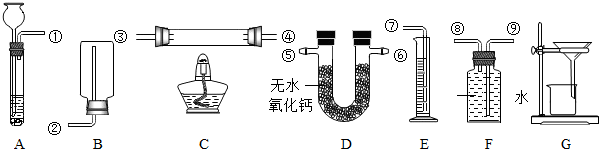
【药品】稀硫酸、浓硫酸、氧化铜
【分析与思考】同学们通过充分“交流-分析-讨论”后一致认为,设计以下三种实验方案可测出黄铜中锌的质量分数.C装置中,提供热源的仪器名称是 ,三种方案都必需选用的药品是 .同学们用过量该药品与称取的ag黄铜粉样品进行充分反应后,实验中测定了以下数据:①测定生成H2的体积bL(已知氢气的密度);
②过滤、洗涤、烘干后,测定漏斗中剩余固体的纯净质量为Cg;
③充分反应后,测定A装置中仪器和药品总质量减少了d克.
【方案一】小悦同学仅选用一个实验装置A进行实验,用测定数据③,通过计算可求出黄铜中锌的质量分数为(写计算结果) 装置A中发生反应的化学方程式为
【方案二】小华同学选用两个装置 (填装置编号,以下同)进行实验,并用测定数据 (填数据编号,以下同),通过计算也求出了黄铜中锌的质量分数.
【方案三】小琳同学选用三个实验装置进行实验,装置连接的顺序是(用装置接口处的编号表示) ,并用测定的数据 ,通过计算也求出了黄铜中锌的质量分数.
【反思与评价】同学们对上述三种实验方案进行了综合评价,一致认为方案 简单易行.

【药品】稀硫酸、浓硫酸、氧化铜
【分析与思考】同学们通过充分“交流-分析-讨论”后一致认为,设计以下三种实验方案可测出黄铜中锌的质量分数.C装置中,提供热源的仪器名称是
②过滤、洗涤、烘干后,测定漏斗中剩余固体的纯净质量为Cg;
③充分反应后,测定A装置中仪器和药品总质量减少了d克.
【方案一】小悦同学仅选用一个实验装置A进行实验,用测定数据③,通过计算可求出黄铜中锌的质量分数为(写计算结果)
【方案二】小华同学选用两个装置
【方案三】小琳同学选用三个实验装置进行实验,装置连接的顺序是(用装置接口处的编号表示)
【反思与评价】同学们对上述三种实验方案进行了综合评价,一致认为方案
考点:实验探究物质的组成成分以及含量,气体的净化(除杂),氢气的制取和检验,书写化学方程式、文字表达式、电离方程式,氢气的化学性质与燃烧实验
专题:科学探究
分析:【方案一】要求锌的质量分数,已知合金的质量,因铜不与酸反应,必须求出锌的质量,根据锌元素的质量分数=
×100%可求得;
【方案二】因铜不反应,可称出铜的质量
【方案三】是利用氢气的量根据化学方程式求锌的质量
| 锌的质量 |
| 合金的质量 |
【方案二】因铜不反应,可称出铜的质量
【方案三】是利用氢气的量根据化学方程式求锌的质量
解答:解:
【分析与思考】C装置中,提供热源的仪器名称是酒精灯,三种方案都必需选用的药品是稀硫酸.
故答案为:酒精灯,稀硫酸.
【方案一】“A装置中仪器和药品总质量减少了d克”根据质量守恒定律应是放出的氢气的质量;
设锌的质量锌的质量为X
Zn+H2SO4═ZnSO4+H2↑
65 2
X dg
=
x=32.5dg
黄铜中锌的质量分数为:
×100%=
×100%
故答案为:
×100%、Zn+H2SO4═ZnSO4+H2↑;
【方案二】因铜不反应,可称出铜的质量,用总质量减去铜的质量,可进一步求得锌的质量.
故答案为:A、G;②.
【方案三】“小琳同学选用三个实验装置进行实验”可确定是利用氢气的量求锌的质量;
故答案为:①→⑧→⑨→⑦;①.
【分析与思考】C装置中,提供热源的仪器名称是酒精灯,三种方案都必需选用的药品是稀硫酸.
故答案为:酒精灯,稀硫酸.
【方案一】“A装置中仪器和药品总质量减少了d克”根据质量守恒定律应是放出的氢气的质量;
设锌的质量锌的质量为X
Zn+H2SO4═ZnSO4+H2↑
65 2
X dg
| 65 |
| x |
| 2 |
| dg |
x=32.5dg
黄铜中锌的质量分数为:
| 32.5dg |
| ag |
| 32.5d |
| a |
故答案为:
| 32.5d |
| a |
【方案二】因铜不反应,可称出铜的质量,用总质量减去铜的质量,可进一步求得锌的质量.
故答案为:A、G;②.
【方案三】“小琳同学选用三个实验装置进行实验”可确定是利用氢气的量求锌的质量;
故答案为:①→⑧→⑨→⑦;①.
点评:本题考查了图示和化学反应相结合的通过化学方程式进行计算,问题难度逐渐加大;解答本题的关键是能够从字意中找出数量关系,掌握反应的情况;对学生理解的能力要求较高.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目