题目内容
7.铁、铜等金属在我们的生活和生产中应用很广.(1)制造汽车所用的钢材是铁(填“铁”或“铜”)的合金.为保护汽车的金属外壳,表面通常喷一层油漆,其主要作用是隔绝空气和水,防止金属锈蚀.
(2)某工厂利用废铁丝、硫酸铜废液(含硫酸亚铁)和废铜粉制备硫酸铜晶体.具体过程如下:

①废铁丝投入到硫酸铜废液中发生反应的化学方程式为Fe+CuSO4=FeSO4+Cu,废铁丝在投入硫酸铜废液前需用稀H2SO4进行处理,其目的是除去铁丝表层的氧化物.
②上述转化完成后,通过操作Ⅰ得到铜粉,在铜粉转化为硫酸铜溶液的过程中,以下反应能够发生且与该过程有关的是AD.
A.2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuOB.Cu+FeSO4=CuSO4+Fe
C.Cu+H2SO4=CuSO4+H2↑D.CuO+H2SO4=CuSO4+H2O.
分析 (1)根据铁的合金以及铁生锈的条件来分析;
(2)根据金属活动性顺序的意义进行分析,在金属活动性顺序中,氢前的金属能与酸发生置换反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,金属氧化物能与酸反应生成盐和水.
解答 解:(1)钢是铁的合金,铁在与水和氧气同时存在时容易生锈.故填:铁;空气和水;
(2)①废铁丝表面有锈,需将铁锈用酸除掉,铁在铜的前面,能将硫酸铜中的铜置换出来,故填:Fe+CuSO4=FeSO4+Cu,除去铁丝表层的氧化物;
②铜能与氧气反应生成氧化铜,氧化铜能与酸反应生成铜盐和水,故填:AD.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
17.欲除去不纯物质中的杂质(括号内为杂质),所用试剂和方法均正确的是( )
| 选项 | 待提纯物质 | 选用试剂 | 操作方法 |
| A | Na2CO3(Na2SO4) | 氯化钡 | 溶解、过滤、洗涤 |
| B | CaO(CaCO3) | 盐酸 | 蒸发、结晶 |
| C | CO2(CO) | 氧气 | 点燃 |
| D | Cu(Fe) | 稀硫酸 | 过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
15.化学实验中,人的五官起着非常重要的作用,下列五官的使用符合实验要求的是( )
| A. |  鼻子闻 | B. |  耳朵听 | C. |  嘴巴吹 | D. |  眼睛看 |
2.下列各实验方案中,可行的是( )
| A. | 用加水溶解、过滤、蒸发的方法,分离氯化钙中混有的碳酸钙粉末 | |
| B. | 用铜丝、银丝、硝酸亚铁溶液,验证铁、铜、银的金属活动性顺序 | |
| C. | 用点燃的方法除去二氧化碳中混有的少量一氧化碳 | |
| D. | 用水区别氢氧化钠、氯化钠、硝酸铵固体 |
3.下列反应是能进行的,没沉淀、无气体生成的复分解反应的是( )
| A. | 硝酸和氧化钙 | B. | 硫酸钠和氯化钡 | C. | 盐酸和氢氧化铝 | D. | 铁和硫酸铜 |
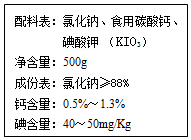 如图是某厂生产的加钙碘盐包装袋商标的部分内容.请仔细阅读后回答以下问题:
如图是某厂生产的加钙碘盐包装袋商标的部分内容.请仔细阅读后回答以下问题: