题目内容
10.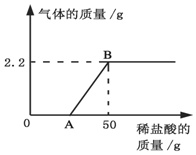 某兴趣小组在实验室发现一瓶敞口久置的氢氧化钠固体.为测定氢氧化钠的变质情况,他们取9.3g变质的氢氧化钠样品于烧杯中,加人42.9g水使其完全溶解,再向烧杯中滴加稀盐酸至过量.测得生成气体质量与所加稀盐酸质量关系如图所示.
某兴趣小组在实验室发现一瓶敞口久置的氢氧化钠固体.为测定氢氧化钠的变质情况,他们取9.3g变质的氢氧化钠样品于烧杯中,加人42.9g水使其完全溶解,再向烧杯中滴加稀盐酸至过量.测得生成气体质量与所加稀盐酸质量关系如图所示.请计算:
(1)9.3g样品中碳酸钠的质量.
(2)B点时,烧杯内溶液的溶质质量分数.(计算结果精确至0.1%)
分析 氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,氢氧化钠能和稀盐酸反应生成氯化钠和水,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)设:9.3g样品中碳酸钠的质量为x,生成氯化钠的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 117 44
x y 2.2g
$\frac{106}{x}$=$\frac{117}{y}$=$\frac{44}{2.2g}$,
x=5.3g,y=5.85g,
答:9.3g样品中碳酸钠的质量是5.3g.
(2)设:氢氧化钠与盐酸反应生成氯化钠的质量为z,
NaOH+HCl═NaCl+H2O,
40 58.5
9.3g-5.3g z
$\frac{40}{9.3g-5.3g}$=$\frac{58.5}{z}$,
z=5.85g,
B点时,烧杯内溶液的溶质质量分数为:$\frac{5.85g+5.85g}{9.3g+42.9g+50g-2.2g}$×100%=11.7%,
答:B点时,烧杯内溶液的溶质质量分数为11.7%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案
相关题目
1.除去下列物质中的杂质所选用的试剂及操作方法正确的一组是( )
| 物质 | 杂质 | 除杂所用试剂和方法 | |
| A | CO2 | HCl气体 | 通过NaOH溶液和浓硫酸 |
| B | NaOH溶液 | Ca(OH)2溶液 | 先加入过量Na2CO3的溶液,再过滤 |
| C | 铁粉 | AgNO3粉末 | 加入足量水,搅拌、过滤、晾干 |
| D | NaCl粉末 | Na2CO3粉末 | 加入适量的稀盐酸,再蒸发 |
| A. | A | B. | B | C. | C | D. | D |
5.将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,将所得滤渣放入稀盐酸中,有气泡产生,下列说法错误的是( )
| A. | 滤液中最多含有两种溶质 | |
| B. | 滤液中一定含有Zn (NO3)2,可能含有Fe (NO3)2 | |
| C. | 若反应后所得滤液呈无色,则滤渣中一定含有Fe和Ag,一定没有Zn | |
| D. | 滤渣里一定含有Fe和Ag,可能含有Zn |
15.下列实验设计不能达到目的是( )
| A. |  鉴别碳酸钠和氢氧化钠溶液 | B. | 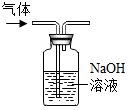 除去CO2中的氯化氢气体 | ||
| C. |  干燥CO2 | D. |  验证化学反应前后质量守恒 |
19.下列关于微粒的说法正确的是( )
| A. | 物质都是由分子构成的 | |
| B. | 构成物质的微粒是在不停地运动的 | |
| C. | 原子和离子不能相互转化 | |
| D. | 热涨冷缩是由于微粒大小发生了变化 |
20.按物质分类的方法,对下列物质进行分类,错误的是( )
| A. | 单质:氧气、汞 | B. | 混合物:空气、海水 | ||
| C. | 碱:烧碱、纯碱 | D. | 盐:硝酸钾、硫酸铁 |
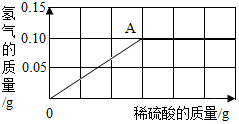 为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算:
为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算: 如图是甲、乙、丙三种物质的溶解度曲线,回答下列问题:
如图是甲、乙、丙三种物质的溶解度曲线,回答下列问题: