题目内容
6.在加有石蕊的稀硫酸中,加入下列物质的过程中,溶液始终显红色的是( )| A. | 碳酸钾溶液 | B. | 氧化锌 | C. | 氯化钡溶液 | D. | 锌 |
分析 根据题意,加有石蕊的稀硫酸中,加入下列物质的过程中,溶液始终显红色,说明反应过程中始终存在酸性物质,据此进行分析判断.
解答 解:A、碳酸钾溶液与稀硫酸反应生成硫酸钾、水和二氧化碳,恰好完全反应时,溶液颜色会由红色变为紫色,继续加入碳酸钾溶液,溶液颜色变为蓝色,故选项错误.
B、氧化锌与稀硫酸反应生成硫酸锌和水,恰好完全反应时,溶液颜色会由红色变为紫色,故选项错误.
C、氯化钡溶液与稀硫酸反应生成硫酸钡沉淀和盐酸,生成的盐酸显酸性,溶液始终显红色,故选项正确.
D、锌与稀硫酸反应生成硫酸锌和氢气,恰好完全反应时,溶液颜色会由红色变为紫色,故选项错误.
故选:C.
点评 本题难度不大,掌握酸的化学性质、石蕊溶液的性质是正确解答本题的关键.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
16.下列说法正确的是( )
| A. | 分子是够成物质的最小微粒 | B. | 元素的化学性质由最外层电子决定 | ||
| C. | 一种元素只能够成一种单质 | D. | 同种元素,质子数等于电子数 |
17.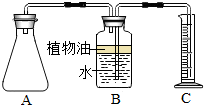 小明买了一种“汽泡爽”的冲调饮料.
小明买了一种“汽泡爽”的冲调饮料.
小明阅读资料发现:“汽泡爽”原料中的柠檬酸和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,3NaHCO3+C6H8O7=C6H5O7Na3+3H2O+3CO2↑
(1)小明想探究加水温度对产生气体量的影响,小明设计了如下实验方案.
在老师的帮助下,小明采用相同的两套实验装置(如图)分别完成上述实验,在A中加入水,再加入一袋“汽泡爽”,迅速塞紧胶塞.量筒C用于收集A中产生的气体所排出的液体,冷却至室温后读取数据.B中油层的作用是防止二氧化碳气体溶解在水中
(2)通过实验,小明测得:a=64mL,b=82mL,由此获得结论:
“汽泡爽”产生气体的量与加水温度有关系.但是老师看到小
明的实验报告后却指出:两套装置中,“汽泡爽”产生气体的 A B C
总量应该近似相等,与温度关系不大,其本质原因是反应物质量没变.
(3)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是不断摇动锥形瓶A,继续收集气体并测量体积.
 小明买了一种“汽泡爽”的冲调饮料.
小明买了一种“汽泡爽”的冲调饮料.小明阅读资料发现:“汽泡爽”原料中的柠檬酸和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,3NaHCO3+C6H8O7=C6H5O7Na3+3H2O+3CO2↑
(1)小明想探究加水温度对产生气体量的影响,小明设计了如下实验方案.
| 实验序号 | 加入水的体积 | 加入水的温度 | 收集到的气体的体积 |
| 1 | 200mL | 15℃ | a(待记录) |
| 2 | 200mL | 50℃ | b(待记录) |
(2)通过实验,小明测得:a=64mL,b=82mL,由此获得结论:
“汽泡爽”产生气体的量与加水温度有关系.但是老师看到小
明的实验报告后却指出:两套装置中,“汽泡爽”产生气体的 A B C
总量应该近似相等,与温度关系不大,其本质原因是反应物质量没变.
(3)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是不断摇动锥形瓶A,继续收集气体并测量体积.
14.据英国《自然》杂志网站2月5日报道,美国科学家使用特殊的催化剂,在阳光下将水变成了可燃的甲烷,这让饱受能源枯竭威胁的人类看到了希望.帮助他们完成这一转化的是一个小小的二氧化钛(TiO2)纳米管.科学家们用这种纳米管催化水蒸气和二氧化碳,结果得到了甲烷(一种碳氢化合物,是天然气、沼气、煤气等的主要成分).则下列说法中错误的是( )
| A. | 从化学原理上讲,这一反应没有违背质量守恒定律 | |
| B. | 甲烷是一种有机物,它能在空气中燃烧 | |
| C. | 二氧化钛是一种金属氧化物,反应前后它的质量不变 | |
| D. | 这一反应是一个化合反应 |
1.下列离子组能在pH=1的无色溶液中大量共存的是( )
| A. | NO3- Fe3+ Na+ OH- | B. | K+ SO42- Na+ NO3- | ||
| C. | Cl- K+ SO42+ Ba2+ | D. | Ca2+ Cl- CO32- Na+ |
16.下列叙述中,不符合实验事实的是( )
| A. | 在K2CO3、K2SO4、AgNO3三种溶液中分别滴入BaCl2溶液,都有白色沉淀生成 | |
| B. | 将SO3,加入到滴有石蕊试液的蒸馏水中,溶液显红色 | |
| C. | 未密封保存的苛性钠遇盐酸有气体生成 | |
| D. | 将稀硫酸溶液加入到某固体粉末中,有无色气体产生,该固体粉末一定是金属 |
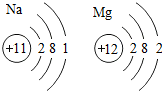 )推知,金属Na、Mg性质不同的原因是最外层电子数不同(合理即可);一氧化碳和二氧化碳性质不同的原因是分子构成不同(合理即可).由此可见,物质的结构决定物质的性质.
)推知,金属Na、Mg性质不同的原因是最外层电子数不同(合理即可);一氧化碳和二氧化碳性质不同的原因是分子构成不同(合理即可).由此可见,物质的结构决定物质的性质.