题目内容
下列化学方程式符合题意且书写正确的是
A. 正常雨水呈酸性的原因:CO2+H2O═H2CO3
B. 铜粉在氧气中加热:Cu+O2 CuO2
CuO2
C. 实验室制取氧气:2H2O2 2H2O+O2↑
2H2O+O2↑
D. 证明铁能与盐酸反应:2Fe+6HCl═2FeCl3+3H2↑
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案硝酸钾的溶解度如下图所示,有关叙述正确的是( )
温度(℃) | 20 | 30 | 40 | 50 | 60 |
溶解度(g/100g水) | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
A. 20℃时,可配成50g35%的硝酸钾饱和溶液
B. 30℃和50℃时,等质量的硝酸钾饱和溶液,所含水的体积,前者大于后者
C. 40℃时,50g硝酸钾饱和溶液降温至20℃,析出固体的质量为32.3g
D. 60℃时,50g硝酸钾饱和溶液中,溶质与溶剂的质量比为11:21
化工厂化验员用铁粉处理硫酸亚铁和硫酸铜混合溶液,回收铜粉和硫酸亚铁溶液,数据记录如下:
铁 | 铜 | 硫酸铜 | 硫酸亚铁 | |
反应前 | 10g | 0g | 混合溶液90g | |
反应后 | 4.4g | 未测 | 溶质质量分数为20% | |
求:(1)反应中消耗铁的质量是______g;
(2)反应后得到铜的质量为________g;
(3)原溶液中硫酸亚铁的质量为________g。
为分析某由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该混合物各20 g,分别缓慢加入到50 g、100 g、150 g某稀硫酸中,测得三组实验数据如表:
组别 | 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 |
稀硫酸的质量/g | 50 | 100 | 150 |
溶解固体的质量/g | 10.0 | 16.0 | 16.0 |
根据实验及有关数据进行分析与计算:
(1)第Ⅰ组实验中反应物______________(填“氧化铜”“稀硫酸”或“氧化铜与稀硫酸”)反应完。
(2)20 g样品中含氧化铜的质量为________g。
(3)根据第Ⅰ组数据计算所用的稀硫酸溶质的质量分数(写出计算过程)。
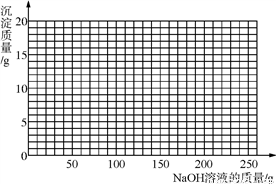
(4)将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,画出在该混合溶液中加入10% NaOH溶液的质量与生成沉淀质量变化关系的曲线图。