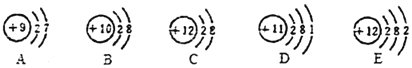题目内容
若金属锰在金属活动性顺序中位于铝和锌之间,则下列反应不能发生的是( )(提示:MnSO4溶于水)
A. Mn+2HCl=MnCl2+H2↑
B. Mg+MnSO4=MgSO4+Mn
C. 2Al+3MnSO4=Al2(SO4)3+3Mn
D. Fe+MnSO4=FeSO4+Mn
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案某兴趣小组对石灰石样品进行如下实验取12g样品放入烧杯中,将100g稀盐酸分4次加入到烧杯中,充分反应后(杂质不溶于水,也不与酸反应),测得剩余固体的质量记录如下。请计算:
次数 | 1 | 2 | 3 | 4 |
加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
剩余固体的质量/g | 8 | 4 | 2 | 2 |
求:
(1)样品中碳酸钙的质量为_____g:
(2)第4次加入稀盐酸后所得溶液中CaCl2的质量分数_______。(写出计算过程,最终结果保留0.1%)。
下表物质中含有少量杂质,其中除杂方法正确的是
物质 | 杂质 | 除去杂质的方法 | |
A | CaCl2溶液 | HCl | 滴入碳酸钠溶液 |
B | CO2 | O2 | 通过灼热的铜网 |
C | NaOH | Na2CO3 | 加入稀盐酸至不再产生气泡 |
D | CuO | Cu | 加足量稀盐酸,充分搅拌后再过滤 |
A. A B. B C. C D. D
某化学兴趣小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后瓶中残留废液进行探究。
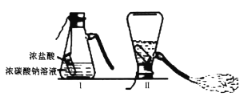
(提出问题)废液中所含溶质是什么?
(猜想与假设)
猜想1:废液中的溶质可能是NaCl、Na2CO3和HCl。
猜想2:废液中的溶质只有NaCl。
猜想3:废液中的溶质是NaCl和HCl。
猜想4:废液中的溶质是_________。
(讨论与交流)
小明认为猜想1无需验证就知道是错误的,他的理由是_______。(请用化学方程式说明)
(实验与结论)
(1)小亮同学为验证猜想3,取少量废液装入试管中,然后滴入酚酞溶液,发现酚酞溶液不变色,于是小亮认为猜想3正确。他的结论错误理由是__________。
请你另设计实验方案验证猜想3:
实验步骤 | 实验现象 | 实验结论 |
__________ | ______ | 猜想3正确 |
(2)验证猜想4,可选用的的试剂有___________。
A.酚酞溶液 B.氢氧化钾溶液 C.稀硫酸 D.氯化钡溶液。
下列事实与相应的解释不一致的是( )
选项 | 现 象 | 解释 |
A | 铁比铝容易生锈 | 铁比铝的活泼性强 |
B | 氯化铜溶液、硫酸铜溶液、硝酸铜溶液呈现蓝色 | 溶液中含有铜离子 |
C | 氢氧化钠溶液显碱性 | 溶液中存在大量OH- |
D | 铁放入硫酸铜溶液中,有红色固体析出 | 铁的活动性比铜强 |
A. A B. B C. C D. D