题目内容
在Fe2(SO4)3和FeSO4的固体混合物中,如果硫元素的质量分数为a%,则铁元素的质量分数为( )
| A、0.31a% |
| B、(100-3a)% |
| C、(100-4a)% |
| D、2.25a% |
考点:元素的质量分数计算
专题:化学式的计算
分析:根据FeSO4和Fe2(SO4)3两物质的组成特点,可知混合物中S元素与O元素的质量比为1:2,混合物中硫元素的质量分数为22%则混合物中O元素质量分数为44%,则可计算混合物中铁元素质量分数.
解答:解:
在FeSO4和Fe2(SO4)3组成的混合物中,硫元素与氧元素的质量比=32:(16×4)=1:2,
由于混合物中硫元素的质量分数为a%,则混合物中氧元素的质量分数=a%×2=2a%
则混合物中铁元素的质量分数=1-a%-2a%=(100-3a)%
故选B.
在FeSO4和Fe2(SO4)3组成的混合物中,硫元素与氧元素的质量比=32:(16×4)=1:2,
由于混合物中硫元素的质量分数为a%,则混合物中氧元素的质量分数=a%×2=2a%
则混合物中铁元素的质量分数=1-a%-2a%=(100-3a)%
故选B.
点评:根据混合物组成中两化合物的中组成元素的特别关系,确定混合物中元素的质量分数,此类问题通过存在这种特点.

练习册系列答案
相关题目
物质的三种状态中,微粒间距离最大的是( )
| A、气态 | B、固态 |
| C、液态 | D、不能判断 |
下图所示实验操作不正确的是( )
A、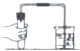 检查装置气密性 |
B、 取粉末状固体药品 |
C、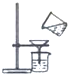 过滤 |
D、 取液体药品 |
集气瓶中装满某气体,可能是下列气体中的一种:①二氧化碳 ②氢气 ③空气 ④氮气.将燃着的木条伸入瓶中,火焰立即熄灭,则该瓶气体可能是( )
| A、①或② | B、②或③ |
| C、①或④ | D、③或④ |
下列关于分子、原子、离子的说法中,错误的是( )
| A、分子能再分,原于不能再分 |
| B、原子一定由质子、电子构成的 |
| C、分子、原子、离子都能构成物质 |
| D、分子、原子都能保持所构成物质的化学性质 |
能证明分子是由原子结合而成的实验事实是( )
| A、铁矿石研磨成粉末 |
| B、水加热到沸腾变成气体 |
| C、能在公园外闻到花香 |
| D、加热氧化汞有水银(汞)生成 |