题目内容
20.小新用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应).操作过程如下:请计算: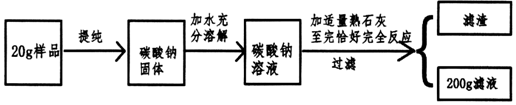
(1)20g样品中含碳酸钠的质量为10.6g;
(2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程) (温馨提示:反应的化学方程式:Ca(OH)2+Na2CO3=CaCO4↓+2NaOH)
分析 根据样品质量及其碳酸钠的质量分数可以计算碳酸钠的质量,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)20g样品中含碳酸钠的质量为:20g×53%=10.6g,
故填:10.6.
(2)设反应后生成氢氧化钠的质量为x,
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
106 80
10.6g x
$\frac{106}{10.6g}$=$\frac{80}{x}$,
x=8g,
反应后所得滤液中氢氧化钠的质量分数为:$\frac{8g}{200g}$×100%=4%,
答:反应后所得滤液中氢氧化钠的质量分数为4%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
10.抗癌新药西达本胺的化学式为C22H19FN4O2,下列关于西达本胺的说法中正确的是( )
| A. | 西达本胺是混合物 | |
| B. | 西达本胺有48个原子 | |
| C. | 西达本胺的相对分子质量为48 | |
| D. | 西达本胺由碳、氢、氟、氮、氧五种元素组成 |
8.下列归纳和总结完全正确的一组是( )
| A.对安全的认识 | B.用“化学”眼光分析 |
| ①点燃可燃性气体前一定要验纯 ②煤气泄漏立即打开排气扇 ③煤矿矿井要保持通风、严禁烟火 | ①洗涤剂去除油污是因为乳化作用 ②用适量的熟石灰可中和土壤的酸性 ③用水灭火是降低温度至可燃物的着火点以下 |
| C.化学与资源 | D.对概念的理解 |
| ①防止金属腐蚀是保护金属资源的途径之一 ②煤、石油、天然气都是可再生能源 ③海洋中蕴藏着丰富的化学资源 | ①能改变反应速率的物质,不一定是催化剂 ②只有单质和化合物生成的反应一定是置换反应 ③含氧元素的化合物一定是氧化物 |
| A. | A | B. | B | C. | C | D. | D |
5.下列方法中不能达到目的是( )
| A. | 用沉淀法除氢氧化钠中的硝酸钾 | |
| B. | 用结晶法除硝酸钾中少量的氯化钠 | |
| C. | 用碳酸氢钠溶液除二氧化碳中的氯化氢气体 | |
| D. | 用过滤法除粗盐中不溶性杂质 |
12.下列图示实验操作正确的是( )
| A. | 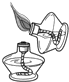 点燃酒精灯 | B. |  向试管中加固体粉末 | ||
| C. | 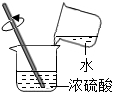 浓硫酸稀释 | D. | 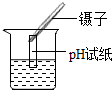 测定溶液的pH |
9.120℃时,取3g有机物R在氧气中完全燃烧,产物只有CO2和H2O.将其燃烧产物依次通过足量的浓硫酸和足量的澄清石灰水中,最终浓硫酸增重1.8g;澄清石灰水中产生10g沉淀.下列判断正确的是( )
| A. | R的化学式一定是CH2O 中 | |
| B. | 6g R完全燃烧消耗氧气6.4g | |
| C. | R中碳元素的质量分数约为85.7% | |
| D. | R仅由C、H两种元素组成,其质量比为6:1 |
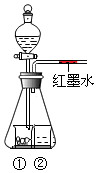 某同学做了如图所示的趣味实验:分液漏斗中盛有水,导管中有一段红墨水,①号烧杯中盛有硝酸铵固体,②号烧杯中盛有饱和硝酸钾溶液,缓缓打开分液漏斗活塞,一段时间后观察到什么现象?并解释出现此现象的原因.
某同学做了如图所示的趣味实验:分液漏斗中盛有水,导管中有一段红墨水,①号烧杯中盛有硝酸铵固体,②号烧杯中盛有饱和硝酸钾溶液,缓缓打开分液漏斗活塞,一段时间后观察到什么现象?并解释出现此现象的原因.