题目内容
18.实验室配制100g 10%的NaCl溶液,不需要用到的仪器是( )| A. | 酒精灯 | B. | 托盘天平 | C. | 胶头滴管 | D. | 烧杯 |
分析 实验室配制100g10%的NaCl溶液操作步骤分别是:计算、称量、溶解,根据各操作所需要使用的仪器,判断所列仪器是否需要.
解答 解:A、配制100g10%的NaCl溶液的过程中,不需要进行加热,则不需要使用酒精灯,该组仪器不合适,故选项正确.
B、配制100g10%的NaCl溶液的过程中,托盘天平用于称取固体氯化钠,故选项错误.
C、配制100g10%的NaCl溶液的过程中,量筒与胶头滴管用于准确量取水,故选项错误.
D、配制100g10%的NaCl溶液的过程中,烧杯用于完成溶解操作,故选项错误.
故选:A.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤(计算、称量、溶解)、所需的仪器是正确解答本题的关键.

练习册系列答案
相关题目
6.小明同学利用一瓶敞口放置已久的NaOH溶液进行了一些实验探究.
[提出问题]这瓶NaOH溶液变质程度如何呢?
[提出猜想]小明的猜想:NaOH溶液部分变质
[实验探究]小明设计了如下实验来验证自己的猜想,请根据表中内容填写实验时的现象.
[实验反思]
(1)下列物质①Ca(OH)2溶液 ②Ba(NO3)2溶液 ③BaCl2溶液,能替代小明实验中CaCl2溶液的是②③
(2)请用化学方程式表示氢氧化钠溶液变质的原因2NaOH+CO2═Na2CO3+H2O
[拓展应用]现向烧杯中加入100g这种已部分变质的NaOH溶液,再滴加溶质质量分数为11.1%的CaCl2溶液100g,产生沉淀质量与所加CaCl2溶液质量的关系如图所示.
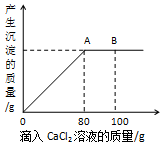
(1)B点处所得溶液中溶质为NaCl和CaCl2 (写化学式)
(2)求反应结束后烧杯中沉淀的质量.
[提出问题]这瓶NaOH溶液变质程度如何呢?
[提出猜想]小明的猜想:NaOH溶液部分变质
[实验探究]小明设计了如下实验来验证自己的猜想,请根据表中内容填写实验时的现象.
| 实验步骤 | 现象 | 结论 |
| 取少量NaOH溶液样品于试管中,先滴加足量CaCl2溶液,然后再滴加酚酞试液 | NaOH部分变质 | |
(1)下列物质①Ca(OH)2溶液 ②Ba(NO3)2溶液 ③BaCl2溶液,能替代小明实验中CaCl2溶液的是②③
(2)请用化学方程式表示氢氧化钠溶液变质的原因2NaOH+CO2═Na2CO3+H2O
[拓展应用]现向烧杯中加入100g这种已部分变质的NaOH溶液,再滴加溶质质量分数为11.1%的CaCl2溶液100g,产生沉淀质量与所加CaCl2溶液质量的关系如图所示.

(1)B点处所得溶液中溶质为NaCl和CaCl2 (写化学式)
(2)求反应结束后烧杯中沉淀的质量.
13.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 化合物是由不同种元素组成的,所以由不同种元素组成的纯净物一定是化合物 | |
| B. | 原子是不带电的微粒,所以不带电的微粒一定是原子 | |
| C. | 有机物是含碳元素的化合物,所以含碳元素的化合物都是有机物 | |
| D. | 铝的化学性质比较活泼,所以在空气中铝比铁更容易被锈蚀 |
10.下列实验现象的描述不正确的是( )
| A. | 把二氧化碳通入石蕊溶液,溶液变红 | |
| B. | 硫在空气中燃烧生成二氧化硫 | |
| C. | 电解水生成氢气和氧气的体积比是2:1 | |
| D. | 打开浓盐酸的瓶盖,瓶口出现大量白雾 |
7.下列图象能正确反映对应的变化关系的是( ) 

| A. | 常温下,向硝酸钾的不饱和溶液中加入硝酸钾晶体 | |
| B. | 将生锈严重的铁钉加入到足量的稀盐酸中 | |
| C. | 向一定质量的稀盐酸溶液中不断加入CaCO3 | |
| D. | 将等质量的镁和锌分别加入到过量、等质量分数的稀盐酸中 |
8.为了测定乙烯(C2H4)在氧气不足时的燃烧产物,将一定量的乙烯和氧气置于一个密闭容器中引燃,测得反应前后各物质的质量如表:
(1)a值是1.4.
(2)该反应的化学方程式为3C2H4+8O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+4CO2+2CO.
| 物质 | 乙烯 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 2.1 | 6.4 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 2.7 | 4.4 | a |
(2)该反应的化学方程式为3C2H4+8O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+4CO2+2CO.
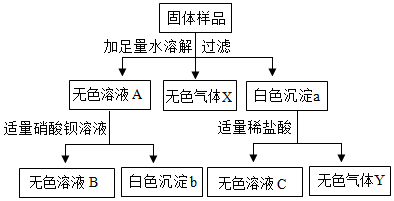 某粉末状物质,可能含有氯化钾、硝酸铵、硫酸镁、氢氧化钠、氢氧化铜、碳酸钙中的一种或几种,为探究其成分,实验流程如下,回答问题.
某粉末状物质,可能含有氯化钾、硝酸铵、硫酸镁、氢氧化钠、氢氧化铜、碳酸钙中的一种或几种,为探究其成分,实验流程如下,回答问题.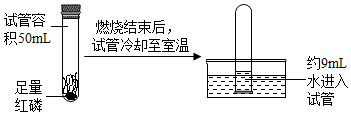 磷的燃烧反应在生产生活中有着广泛的应用价值.
磷的燃烧反应在生产生活中有着广泛的应用价值.