题目内容
某同学为了测定实验室氯酸钾样品的纯度,取2.5克该样品与0.5克二氧化锰混合.加热该混合物T1时间后(假设杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加热时间T2,T3,T4后剩余固体的质量,记录数据如下表:
(1)加热T3时间后,氯酸钾是否已经反应完全? (填“是”或“否”);
(2)求样品中氯酸钾的质量.
(3)求样品中氯酸钾的纯度(用百分数表示)?
| 加热时间 | T1 | T2 | T3 | T4 |
| 剩余固体质量/克 | 2.12 | 2.08 | 2.04 | 2.04 |
(2)求样品中氯酸钾的质量.
(3)求样品中氯酸钾的纯度(用百分数表示)?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据氯酸钾受热分解生成氧气,加热T3时间后,固体的质量不再减少进行解答;
(2)根据根据质量守恒定律,在反应剩余固体不再减小时,与原固体的质量差即为放出氧气的质量,利用反应的化学方程式,由放出氧气的质量计算出样品中氯酸钾的质量即可;
(3)再利用纯度公式计算该样品中氯酸钾的纯度进行解答.
(2)根据根据质量守恒定律,在反应剩余固体不再减小时,与原固体的质量差即为放出氧气的质量,利用反应的化学方程式,由放出氧气的质量计算出样品中氯酸钾的质量即可;
(3)再利用纯度公式计算该样品中氯酸钾的纯度进行解答.
解答:解:(1)氯酸钾受热分解生成氧气,加热T3时间后,固体的质量不再减少,所以加热T3时间后,氯酸钾已经反应完全;故填:是;
(2)氧气的质量为2.5g+0.5g-2.04g═0.96g
设氯酸钾的质量为x
2KClO3
2KCl+3O2↑
245 96
x 0.96g
=
x=2.45g
(3)样品中氯酸钾的纯度=
×100%=98%
答:(2)样品中氯酸钾的质量为2.45g;(3)样品中氯酸钾的纯度为98%.
(2)氧气的质量为2.5g+0.5g-2.04g═0.96g
设氯酸钾的质量为x
2KClO3
| ||
| △ |
245 96
x 0.96g
| 245 |
| x |
| 96 |
| 0.96g |
x=2.45g
(3)样品中氯酸钾的纯度=
| 2.45g |
| 2.5g |
答:(2)样品中氯酸钾的质量为2.45g;(3)样品中氯酸钾的纯度为98%.
点评:分析图表中数据时,要关注造成数据发生变化的原因,分析数据不再改变时所说明的问题,从而发现隐含条件.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
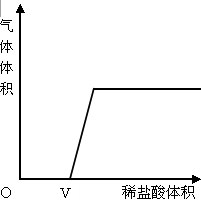 从H2SO4、NaCl、NaOH、Na2CO3、Ba(OH)2几种溶液中取出其中的两种混合,可能的组合有若干种.
从H2SO4、NaCl、NaOH、Na2CO3、Ba(OH)2几种溶液中取出其中的两种混合,可能的组合有若干种.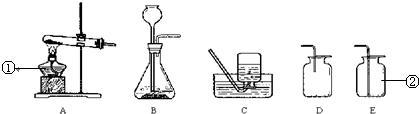
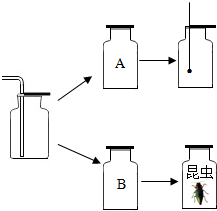 某同学为了探究物质的性质,以氧气为例,做了如下实验:如图所示,先收集了两瓶氧气后正放在桌上,盖好玻璃片,然后用带火星的木条插入A集气瓶中,在B瓶中放入一只昆虫.请回答下列问题.
某同学为了探究物质的性质,以氧气为例,做了如下实验:如图所示,先收集了两瓶氧气后正放在桌上,盖好玻璃片,然后用带火星的木条插入A集气瓶中,在B瓶中放入一只昆虫.请回答下列问题.