题目内容
我国是世界钢铁产量最大的国家,如果炼铁的主要原料是磁铁矿,所用还原剂为一氧化碳。请回答:
(1)上述炼铁的反应不是置换反应的理由是: 。
(2) 根据化学方程式计算:用含Fe3O460%的赤铁矿石800t,理论上可炼出纯铁多少吨?
(1)上述炼铁的反应不是置换反应的理由是:
。
(2) 根据化学方程式计算:用含Fe3O460%的赤铁矿石2320 t,理论上可炼出纯铁多少吨?
(1)由化学方程式可知,反应物中没有单质,故不属于置换反应;故答案为:反应物中没有单质;
(2).设理论上可炼出纯铁的质量为x.
Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
160 112
800t×60% x
∴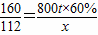 ,解之得:x=336t.
,解之得:x=336t.
答:理论上可炼出纯铁336t.

 阅读快车系列答案
阅读快车系列答案点燃下列各组混合气体,一定不会发生爆炸的是( )
|
| A. | 二氧化碳和氧气 | B. | 一氧化碳和空气 |
|
| C. | 液化石油气和空气 | D. | 天然气和氧气 |
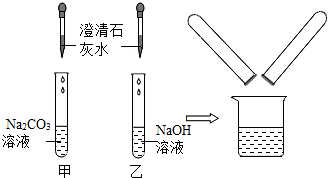
老师为了辨别一瓶失去标签的溶液时碳酸钠还是氢氧化钠进行了如图所示的两个实验,实验结束后,老师将试管中的废液倒入同一个干净的烧杯中茗茗看到废液变浑浊,就对废液进行了过滤,并和几位同学对滤液的成分又进行了探究.
【提出问题】滤液中只含NaOH:
【猜想与假设】
甲同学认为:滤液中只含NaOH
乙同学认为:滤液中可能含有NaOH和Na2CO3
丙同学认为:滤液中可能含有NaOH,Na2CO3和Ca(OH)2
【讨论】
(1)图甲中,发生反应的化学方程式为 ;
(2)你认为上述猜想不合理的是 ,理由是 ;
【实验分析】经过与同学的商量后,茗茗决定针对乙同学的猜想进行实验,实验过程如下表所示,请将表格补充完整
| 实验操作 | 取适量滤液于试管中,向其中加入酸性溶液① |
| 实验现象 | ② |
| 实验结论 | 乙同学的猜想成立 |
20℃时,取甲、乙、丙、丁四种纯净物各20g,分别加入到各盛有50g水的烧杯中,充分溶解(四种物质均不与水反应),其溶解情况如表,下列说法中正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 未溶解固体的质量/g | 4.2 | 2 | 0 | 9.2 |
|
| A. | 丙溶液是不饱和溶液 |
|
| B. | 乙物质在20℃时的溶解度是18克 |
|
| C. | 丁是不易溶于水的物质 |
|
| D. | 20℃时四种物质溶解度的关系为:丙>乙>甲>丁 |
 可以增大硬度防止撞坏
可以增大硬度防止撞坏 (1)甲图中,t2℃时,A、B、C三种物质中,
(1)甲图中,t2℃时,A、B、C三种物质中,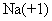 —钠离子
—钠离子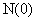 2—氮气中氮元素的化合价为0
2—氮气中氮元素的化合价为0  论。以下类推正确的是( )
论。以下类推正确的是( ) 化碳和氢气都能夺取氧化铜中的氧,所以一氧化碳和氢气都具有还原性
化碳和氢气都能夺取氧化铜中的氧,所以一氧化碳和氢气都具有还原性