题目内容
1.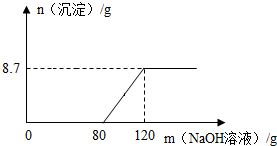 向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示.
向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示.(1)计算氢氧化钠溶液的溶质质量分数
(2)氢氧化钠溶液反应所消耗硫酸溶质的质量为多少克.
分析 稀硫酸和镁反应生成硫酸镁和氢气,硫酸镁和氢氧化钠反应生成氢氧化镁沉淀和硫酸钠,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:设:生成8.7gMg(OH)2消耗的NaOH的质量为x,氢氧化钠溶液反应所消耗硫酸溶质的质量为y,
MgSO4+2NaOH=Mg(OH)2↓+Na2SO4,
80 58
x 8.7g
$\frac{80}{x}$=$\frac{58}{8.7g}$,
x=12g,
氢氧化钠溶液中溶质质量分数为:$\frac{12g}{120g-80g}$×100%=30%,
答:氢氧化钠溶液中溶质质量分数为30%.
H2SO4消耗的NaOH的质量为:80g×30%=24g,
H2SO4+2NaOH=Na2SO4+2H2O,
98 80
y 24g
$\frac{98}{y}$=$\frac{80}{24g}$,
y=29.4g,
答:氢氧化钠溶液反应所消耗硫酸溶质的质量为29.4g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列说法正确的是( )
| A. | 等质量的CO和CO2,CO和CO2中氧元素的质量比为11:14 | |
| B. | 等质量的Al和Mg分别与足量稀硫酸充分反应,生成H2的质量相等 | |
| C. | 等质量的NaHCO3和MgCO3分别与足量稀盐酸充分反应,生成CO2的质量不相等 | |
| D. | 等质量的质量分数均为4%氢氧化钠溶液与稀盐酸充分反应后,所得溶液显中性 |
9.关于水的净化过程描述错误的是( )
| A. | 通过过滤装置除去可溶性杂质 | B. | 通入氯气杀菌消毒 | ||
| C. | 加入明矾使不溶性悬浮物凝聚 | D. | 通过活性炭吸附部分有害物质 |
6.下列各组物质在溶液中能大量共存且形成无色溶液的是( )
| A. | K2CO3 NaCl HCl | B. | CuSO4 H2SO4 NaNO3 | ||
| C. | BaCl2 AgNO3 Na2SO4 | D. | AlCl3 KNO3 Na2SO4 |
3.现有50克浓度为10%的KNO3溶液,要使其浓度增大一倍,可以采用的方法是( )
| A. | 蒸发掉25克水 | B. | 加水溶液变100克 | C. | 增加10克溶质 | D. | 增加6.25克溶质 |
4.对下列实验中出现的异常情况的原因分析,合理的是( )
| A. | 氢氧化钠溶液与盐酸混合时无明显现象,说明它们一定没有反应 | |
| B. | 氯化钙溶液中混有盐酸,加碳酸钙,无气泡产生,说明盐酸已除尽 | |
| C. | 用块状石灰石与稀硫酸制取CO2时,始终收集不满,说明装置一定漏气 | |
| D. | 检验某氢氧化钠溶液是否变质时滴加几滴稀盐酸,没有气泡,说明一定没有变质 |