题目内容
19.将质量相等、溶质质量分数相同的两份稀硫酸分装在甲、乙两个烧杯中,再称取质量相等的铝和锌,把铝放入甲烧杯中,锌放入乙烧杯中,待反应结束后,发现甲烧杯中铝有剩余,乙烧杯中的锌已全部反应,根据此现象推断,下列结论中,正确的是( )| A. | 一定是乙烧杯中产生的氢气多 | |
| B. | 可能是乙烧杯中产生的氢气多 | |
| C. | 一定是甲烧杯中产生的氢气多 | |
| D. | 可能甲、乙两烧杯中产生的氢气一样多 |
分析 因为甲烧杯中铝有剩余,说明稀硫酸已用完,在此反应中产生了足够多的氢气;而乙烧杯中锌已全部反应,说明在此反应中有两种情况可能存在:①稀硫酸已用完,产生了足够的氢气,那么甲乙两烧杯中产生的氢气一样多;②稀硫酸没有全部反应,因此,就没有产生足够的氢气,在此实验中甲烧杯中产生的氢气多.
解答 解:因为甲烧杯中铝有剩余,说明稀硫酸已用完,在此反应中产生了足够多的氢气;而乙烧杯中锌已全部反应,说明在此反应中有两种情况可能存在:①稀硫酸已用完,产生了足够的氢气,那么甲乙两烧杯中产生的氢气一样多;②稀硫酸没有全部反应,因此,就没有产生足够的氢气,在此实验中甲烧杯中产生的氢气多.
我们对实验现象的推断,要充分考虑可能出现的各种现象,全面分析.
A、甲、乙两烧杯中产生的氢气可能一样多,故错误;
B、乙烧杯中产生的氢气最多与烧杯中产生的氢气一样多,故错误;
C、如果乙烧杯中稀硫酸没有全部反应,因此,就没有产生足够的氢气,在此实验中甲烧杯中产生的氢气多,故错误.
D、如果乙烧杯中稀硫酸已用完,产生了足够的氢气,那么甲乙两烧杯中产生的氢气一样多.故正确.
故选D.
点评 本题主要考查学生对完全反应和不完全反应的概念的区别,以及运用知识进行推断的能力.学生需全面分析,才能正确选择.

练习册系列答案
相关题目
10.有一包白色固体,可能含有FeCl3、CaCO3、NaOH、Ba(OH)2、BaCl2、Na2SO4中的几种.为确定其组成,取适量试样进行下列实验.请根据实验现象判断:
①取试样溶于水,搅拌、过滤,得到无色澄清溶液A和白色沉淀B;
②取上述无色澄清溶液A,通入适量的CO2,生成白色沉淀C;
③取上述白色沉淀B,加入过量的稀硝酸,沉淀全部消失.
综合上述实验现象,下列判断正确的是( )
①取试样溶于水,搅拌、过滤,得到无色澄清溶液A和白色沉淀B;
②取上述无色澄清溶液A,通入适量的CO2,生成白色沉淀C;
③取上述白色沉淀B,加入过量的稀硝酸,沉淀全部消失.
综合上述实验现象,下列判断正确的是( )
| A. | 由①得原白色固体中一定不含FeCl3,一定含量有CaCO3 | |
| B. | 由②③得原白色固体中一定含有Ba(OH)2,一定不含量有Na2SO4 | |
| C. | 由实验现象判断,白色固体中至少有3种固体 | |
| D. | 由实验现象判断,白色固体的组成可有5种情况 |
7.通过下列实验操作和现象能得出相应结论的是( )
| 实验操作 | 现 象 | 结 论 | |
| A | 向集满CO2的软塑料瓶中加入约$\frac{1}{3}$ 体积滴有石蕊试液的水,旋紧瓶盖,振荡 | 塑料瓶变瘪, 溶液变红 | CO2能与石蕊 反应 |
| B | 向某无色溶液中滴加氯化钡溶液 | 有白色沉淀 | 无色溶液中 一定含有SO42- |
| C | 向久置于空气中的氢氧化钠溶液 中滴加稀硫酸 | 有气泡 | 氢氧化钠溶液 已变质 |
| D | 把质量相同的镁粉与锌粒同时放入 相同浓度和体积的盐酸中 | 镁粉与盐酸 产生气体更快 | 镁的金属 活动性比锌强 |
| A. | A | B. | B | C. | C | D. | D |
14.分离、提纯是化学实验的重要环节,下列方法中能达到实验目的是C.
| 选项 | 物质(括号内杂质) | 除去杂质的方法 |
| A | CuSO4溶液(H2SO4) | 加足量的铜粉末,过滤 |
| B | CaO(CaCO3) | 加水溶解、过滤 |
| C | CO(CO2) | 通过足量氢氧化钠溶液,并干燥 |
| D | NaOH溶液(Na2SO4) | 加入适量的氢氧化钡溶液,过滤 |
9.下列物质中既存在离子又存在分子的是( )
| A. | 碳酸钠固体 | B. | 金刚石 | C. | 蔗糖溶液 | D. | 石灰水 |
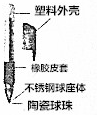 如图是某圆珠笔的示意图:
如图是某圆珠笔的示意图: