题目内容
在实验室用一氧化碳还原2.0 g赤铁矿样品,反应后生成的二氧化碳跟足量的澄清石灰水反应,生成了3.0 g白色沉淀。求赤铁矿样品中Fe2O3的质量分数。
. 解:设生成3.0 g碳酸钙需要二氧化碳 的质量为x
的质量为x
CO2+Ca(OH)2===CaCO3↓+H2O (1分)
44 100
x 3.0 g
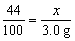 (2分)
(2分)
x= =1.32 g (3分)
=1.32 g (3分)
设生成1.32 g二氧化碳需要Fe2O3的质量为y
Fe2O3+3CO 2Fe+3CO2 (4分)
2Fe+3CO2 (4分)
160 132
y 1.32 g
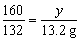 (5分)
(5分)
y=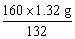 =1.6 g (6分)
=1.6 g (6分)
赤铁矿样品中Fe2O3的质量分数为
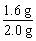 ×100% (7分)
×100% (7分)
=80% (8分)
答:赤铁矿样品中Fe2O3的质量分数为80%。

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案金属是一种重要的材料,人类的生活和生产都离不开金属。下表表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限。
 |  |

K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
 | |||
 | |||
⑴ 根据图中数据和有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列
有关。
①地壳中金属元素的含量;②金属的导电性;③金属的活动性;④金属的延展性;⑤金 属冶炼的难易程度。
属冶炼的难易程度。
⑵ 钢铁的生产和使用是人类文明和社会进步的一个重要标志。请你写出一氧化碳在高温条件下把铁从赤铁矿(主要成分是氧化铁)里还原出来的化学方程式: 。
⑶ 每年世界上钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟 等物质相互反应的结果。
⑷ 铝的活动性比铁强,但铝在空气中却表现出良好的抗腐蚀性,其原因是
 试剂瓶C.块状而又无腐蚀性的药品允许用手直接取用D.加热后的试管冷却后,才用清水冲洗
试剂瓶C.块状而又无腐蚀性的药品允许用手直接取用D.加热后的试管冷却后,才用清水冲洗 C.金黄色的金粉应该属于纳米材料 D.在空气中能自燃的铁粉应该属于纳米材料
C.金黄色的金粉应该属于纳米材料 D.在空气中能自燃的铁粉应该属于纳米材料 A.该元素原子的质子数为14
A.该元素原子的质子数为14 氯化镁、硫酸铜中的两种或两种以上的物质组成的,小红同学为探究其成分,设计并完成了以下实验:
氯化镁、硫酸铜中的两种或两种以上的物质组成的,小红同学为探究其成分,设计并完成了以下实验: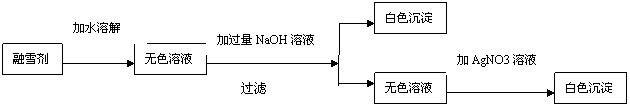
 书写完全正确的是( )
书写完全正确的是( ) MgO2 B.2H2+O2==2H2O
MgO2 B.2H2+O2==2H2O [ ]
[ ]