题目内容
9.20℃时,向X克水中加入18克氯化钠,使其完全溶解得到不饱和溶液,若加热蒸发掉22克水后冷却到原来温度,得到该盐的质量分数为26.5%的饱和溶液(无晶体析出),向该饱和溶液中加入107.2克硝酸银溶液时刚好反应完全.求:(1)20℃时氯化钠的溶解度;
(2)X的值;
(3)反应后溶液中溶质的质量分数.
分析 (1)根据该饱和氯化钠溶液的质量分数进行计算;
(2)根据20℃时氯化钠的溶解度进行解答;
(3)根据氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,然后结合题中的数据进行计算.
解答 解:(1)设20℃时氯化钠的溶解度为x,
26.5%=$\frac{x}{100g+x}$
x=36g;
(2)$\frac{18g}{X-22g}$=$\frac{36}{100g}$
X=72g;
(3)设生成硝酸钠的质量为y,生成氯化银的质量为z,
NaCl+AgNO3=NaNO3+AgCl↓
58.5 170 85 143.5
18g y z
$\frac{58.5}{18g}$=$\frac{85}{y}$=$\frac{143.5}{z}$
y=44.2g
z=26.2g
所以反应后溶液中溶质的质量分数为:$\frac{44.2g}{18g+72g-22g+107.2g}$×100%=25.2%.
故答案为:(1)36g;
(2)72g;
(3)25.2%.
点评 本题主要考查了有关化学方程式和溶解度的有关计算,难度较大,需要认真分析题意即可解答.

练习册系列答案
相关题目
19.下列实验设计不能达到目的是( )
| A. | 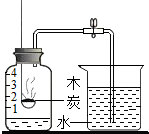 测定空气中氧气含量 | B. | 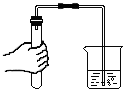 检查装置气密性 | ||
| C. | 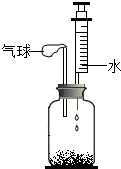 验证反应放热 | D. | 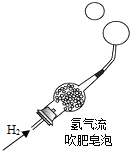 验证氢气密度比空气小 |
17.下列对催化剂的认识错误的是( )
| A. | 催化剂只能加快其他物质的化学反应速率 | |
| B. | 催化剂在化学反应前后的质量不变 | |
| C. | 催化剂的化学性质在化学反应前后不变 | |
| D. | 催化剂能减慢化学反应速率 |
4.下列电离方程式书写正确的是( )
| A. | Na2CO3═Na2++CO32- | B. | H2SO4═2H++SO42- | ||
| C. | CuSO4═Cu++SO4- | D. | ZnCl2═Zn+2+2Cl- |
14.现有X、Y、Z三种金属(Mg、Zn、Cu),把Y投入到X的硫酸盐溶液中,Y溶解而且溶液质量减少;把Z投入到X的硫酸盐溶液中,Z溶解而且溶液质量增加.则X、Y、Z依次是( )
| A. | Mg,Zn,Cu | B. | Cu,Mg,Zn | C. | Zn,Mg,Cu | D. | Cu,Zn,Mg |