题目内容
2.已知赤铁矿的主要成分是氧化铁,其矿石里铁元素为55%,求该铁矿石里氧化铁的质量分数?分析 根据化合物的质量=该化合物中某元素的质量÷该元素的质量分数,进行分析解答.
解答 解:已知赤铁矿的主要成分是氧化铁,其矿石里铁元素为55%,则该铁矿石里氧化铁的质量分数为55%÷($\frac{56×2}{56×2+16×3}×$100%)≈78.6%.
答:该铁矿石里氧化铁的质量分数为78.6%.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.小强同学对样品中碳酸钙的质量分数进行检测,采用的办法如下:取用8g这种石灰石样品,把40g稀盐酸分4次加入,测量过程所得数据见下表(已知石灰石样品中含的杂质不溶于水,不与盐酸反应).请计算:
(1)8g石灰石样品中含有杂质多少克?(2)样品中碳酸钙的质量分数是多少?
(3)下表中m的数值应该为多少?
(4)要得到280kg CaO,需要质量分数为80%的石灰石多少千克?
(化学方程式:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑)
(1)8g石灰石样品中含有杂质多少克?(2)样品中碳酸钙的质量分数是多少?
(3)下表中m的数值应该为多少?
| 序号 | 加入稀盐酸质量(g) | 剩余固体质量(g) |
| 第1次 | 10 | 5 |
| 第2次 | 10 | m |
| 第3次 | 10 | 1.2 |
| 第4次 | 10 | 1.2 |
(化学方程式:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑)
14.现在有一不纯的CaCO3样品(里面只有一种杂质),经测定样品中氧元素的质量分数为46%,则里面含有的杂质可能是( )
| A. | CuO | B. | H2O | C. | CO | D. | Al2O3 |
11.粗盐提纯实验中,蒸发时,下列操作正确的是( )
| A. | 把浑浊的液体倒入蒸发皿中就加热 | B. | 开始析出晶体后用玻璃棒搅拌 | ||
| C. | 蒸发皿中出现大量固体时停止加热 | D. | 待液体蒸干后停止加热 |
14.下列物质在氧气中燃烧,能生成黑色固体的一组是( )
①镁 ②硫 ③铁 ④磷.
①镁 ②硫 ③铁 ④磷.
| A. | ①③ | B. | ③ | C. | ③④ | D. | ③ |
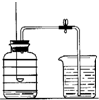 用来测定空气成分的方法很多,图1所示的是小明用红磷在空气中燃烧的测定方法.实验过程是:
用来测定空气成分的方法很多,图1所示的是小明用红磷在空气中燃烧的测定方法.实验过程是: