题目内容
4.现有一包白色粉末,可能是氯化钙,硝酸铜或干燥剂(主要成分是生石灰)中的一种或几种物质组成,为了研究白色粉末的组成,进行了如下实验.(1))将部分放入烧杯中,加适量水充分搅拌后,得到蓝色浊液,得出:粉末中一定含有硝酸铜、干燥剂,可能有氯化钙;
(2)向上述蓝色溶液中滴加氢氧化钠溶液,可观察到有有蓝色沉淀生成,有关的反应的化学方程式为2NaOH+Cu(NO3)2=Cu(OH)2↓+2NaNO3.
分析 根据硝酸铜在溶液中显蓝色,氧化钙和水会生成氢氧化钙,氢氧化钙和硝酸铜会生成氢氧化铜沉淀等知识进行分析.
解答 解:硝酸铜在溶液中显蓝色,氧化钙和水会生成氢氧化钙,氢氧化钙和硝酸铜会生成氢氧化铜沉淀.
(1)将部分放入烧杯中,加适量水充分搅拌后,得到蓝色浊液,得出粉末中一定含有硝酸铜、干燥剂,可能含有氯化钙;
(2)氢氧化钠和硝酸铜会生成蓝色的氢氧化铜沉淀和硝酸钠,实验现象为:有蓝色沉淀生成,化学方程式为:2NaOH+Cu(NO3)2=Cu(OH)2↓+2NaNO3.
故答案为:(1)硝酸铜、干燥剂,氯化钙;
(2)氢有蓝色沉淀生成,2NaOH+Cu(NO3)2=Cu(OH)2↓+2NaNO3.
点评 在解此类题时,首先分析所给混合物中各物质的性质,然后根据题中所给的实验现象进行判断,最后确定混合物的组成成分.

练习册系列答案
相关题目
14.用石灰石、水、纯碱为原料制取烧碱,发生反应的化学方程式有:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑、CaO+H2O═Ca(OH)2、Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,这些反应都不属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
15.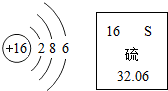 根据如图信息,说法正确的是( )
根据如图信息,说法正确的是( )
 根据如图信息,说法正确的是( )
根据如图信息,说法正确的是( )| A. | 硫属于金属元素 | |
| B. | 硫的相对原子质量为32.06g | |
| C. | 硫原子的核电荷数为16 | |
| D. | 在化学反应中,硫原子容易失去6个电子 |
12.下列关于盐酸的叙述正确的是( )
| A. | 盐酸是挥发性酸 | |
| B. | 胃液里含有少量盐酸会影响健康 | |
| C. | 盐酸能使所有的酸碱指示剂变色 | |
| D. | 盐酸可用于除去碳酸钠中的氯化钠杂质 |