题目内容
加热31.6g KMnO4,当得到3gO2时,剩余固体的成分是( )
| A、K2MnO4和MnO2 |
| B、KMnO4和K2MnO4 |
| C、KMnO4、K2MnO4和MnO2 |
| D、MnO2和KMnO4 |
考点:根据化学反应方程式的计算
专题:推断混合物的可能组成
分析:根据反应的化学方程式,求算出得到3g氧气分解的高锰酸钾的质量,即可知道剩余固体的质量,据此解答.
解答:解:设生成3g氧气需要高锰酸钾的质量为x
2KMnO4
K2MnO4+MnO2+O2↑
316 32
x 3g
=
x≈29.6g
说明高锰酸钾未全部参加反应,故剩余的固体有高锰酸钾、二氧化锰和锰酸钾,观察选项,故选C.
2KMnO4
| ||
316 32
x 3g
| 316 |
| x |
| 32 |
| 3g |
说明高锰酸钾未全部参加反应,故剩余的固体有高锰酸钾、二氧化锰和锰酸钾,观察选项,故选C.
点评:本题考查了根据化学方程式的计算,完成此题的关键是准确书写反应的化学方程式.

练习册系列答案
相关题目
下列化学方程式的书写,完全正确的是( )
| A、CaCO3═CaO+CO2↑ | ||||
| B、Cu+2AgNO3═2Ag+Cu(NO3)2 | ||||
| C、2Fe+6HCl═2FeCl3+3H2↑ | ||||
D、2KMnO4
|
某同学在实验报告中记录下列数据,其中正确的是( )
| A、用25mL量筒量取20.06mL盐酸 |
| B、用托盘天平称取5.25g食盐 |
| C、用100mL烧杯量取80.5mL盐酸 |
| D、用燃烧法测得空气中氧气体积分数为21% |
某地农业科学工作者在进行“酸雨对农业生产影响及其对策的研究”中得出酸雨的pH大小与小麦减产幅度关系的一组数据如下表所示:
根据数据判断,下列说法正确的是( )
| 酸雨的pH | 3.58 | 4.59 | 4.86 |
| 小麦减产(g) | 10 | 5 | 3 |
| A、酸雨的pH越大,小麦减产幅度越大 |
| B、酸雨的pH越小,小麦减产幅度越大 |
| C、酸雨的酸性越弱,小麦减产幅度越小 |
| D、酸雨的酸性越强,小麦减产幅度越小 |
下列化学符号与所表述的意义相符合的是( )
| A、O2--2个氧原子 |
| B、Mg2+--1个镁离子 |
| C、Ca--1个钙元素 |
| D、碳酸钾--KCO3 |
下列各种溶液里的溶质中,在常温下是液体的是( )
| A、碘酒 | B、糖水 |
| C、食盐溶液 | D、酒精溶液 |

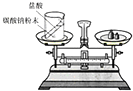 在质量守恒定律探究中,某同学利用右侧的天平称量:
在质量守恒定律探究中,某同学利用右侧的天平称量: