题目内容
5.欲除去氯化钙溶液中含有的少量盐酸,在没有指示剂的条件下可选用的试剂是( )| A. | 苛性钠 | B. | 石灰石 | C. | 生石灰 | D. | 熟石灰 |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、盐酸和苛性钠反应生成氯化钠和水,能除去杂质但引入了新的杂质氯化钠,不符合除杂原则,故选项所采取的方法错误.
B、盐酸能与过量的石灰石粉末反应生成氯化钙、水和二氧化碳,再过滤除去过量的难溶于水石灰石,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、生石灰能与盐酸反应生成氯化钙和水,不好判断反应是否恰好进行,容易引入新的杂质氢氧化钙,故选项所采取的方法错误.
D、熟石灰能与盐酸反应生成氯化钙和水,不好判断反应是否恰好进行,容易引入新的杂质氢氧化钙,故选项所采取的方法错误.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
16.推理和归纳是研究和学习化学的重要方法.以下说法正确是( )
| A. | 分子可以构成物质,但物质不一定由分子构成 | |
| B. | H2O和H2O2的组成元素相同,所以他们的化学性质相同 | |
| C. | 盐中含有金属离子和酸根离子,NH4NO3中没有金属离子,所以不属于盐类 | |
| D. | 酸能使紫色石蕊溶液变红,CO2通入紫色石蕊溶液后溶液变红,所以CO2是酸 |
13.珍爱生命,远离毒品.冰毒是一种毒品,其主要成分是甲基苯丙胺(C10H11N),下列有关甲基苯丙胺的说法中,正确的是( )
| A. | 属于有机物 | B. | 一个分子中原子总数为25 | ||
| C. | 属于混合物 | D. | 在空气中燃烧只生成二氧化碳和水 |
1. 酸溶液和碱溶液混合会发生怎样的变化呢?某班级同学开展如图所示相关的实验.下面是两个小组的实验记录与分析.请根据要求回答问题:
酸溶液和碱溶液混合会发生怎样的变化呢?某班级同学开展如图所示相关的实验.下面是两个小组的实验记录与分析.请根据要求回答问题:
(1)室温下,甲组同学往一定体积10%的氢氧化钠溶液样品中滴加10%的盐酸,反应中溶液温度的变化记录如下:
根据上表数据分析:
①当加入盐酸体积为10mL时,表明NaOH与HCl恰好完全反应.此判断的依据是此时温度上升的最高.
②当加入6mL盐酸时,烧杯中溶液仍然呈红色,该溶液中含有的溶质有酚酞和氯化钠、氢氧化钠.
(2)请你参与完成乙组同学的实验记录与分析.
 酸溶液和碱溶液混合会发生怎样的变化呢?某班级同学开展如图所示相关的实验.下面是两个小组的实验记录与分析.请根据要求回答问题:
酸溶液和碱溶液混合会发生怎样的变化呢?某班级同学开展如图所示相关的实验.下面是两个小组的实验记录与分析.请根据要求回答问题:(1)室温下,甲组同学往一定体积10%的氢氧化钠溶液样品中滴加10%的盐酸,反应中溶液温度的变化记录如下:
| 加入盐酸的体积(V)/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 溶液温度上升(△t)/℃ | 5.6 | 9.8 | 12.1 | 16.3 | 18.5 | 17.1 | 15.2 | 14.6 | 13.5 | 12.6 |
①当加入盐酸体积为10mL时,表明NaOH与HCl恰好完全反应.此判断的依据是此时温度上升的最高.
②当加入6mL盐酸时,烧杯中溶液仍然呈红色,该溶液中含有的溶质有酚酞和氯化钠、氢氧化钠.
(2)请你参与完成乙组同学的实验记录与分析.
| 实验操作 | 实验现象 | 分析与结论 |
| 步骤一:往装有氢氧化钠溶液样品的试管中先滴加2~3滴的 酚酞试液,再逐滴加 入稀盐酸 | 现象一:有气泡产生 现象二:溶液由红色变成无色 | 1.该氢氧化钠溶液样品已变质 2.溶液碱性消失 |
| 步骤二:取步骤一反应后的溶液,然后逐滴加入该氢氧化钠溶液样品 | 现象一:有气泡产生 现象二:溶液开始不变色,后逐渐变成红色 | 1.产生“气泡”这一现象对应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑ 2.所取的步骤一反应后的溶液 pH<7(填“<”、“=”或“>”) |
19.下列说法不正确的是( )
| A. | 利用元素周期表,可查阅元素符号 | |
| B. | 分子可以构成物质,但物质不一定由分子构成 | |
| C. | 汤姆森发现了电子,证实原子是可分的 | |
| D. | 利用相对原子质量表,可直接查出某种元素一个原子的实际质量 |
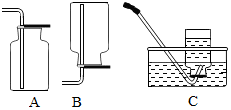 (1)每当电闪雷鸣之时,空气中发生的一种反应为N2+O2═2NO,近空气的密度,如要收集NO应选用下列C装置收集.
(1)每当电闪雷鸣之时,空气中发生的一种反应为N2+O2═2NO,近空气的密度,如要收集NO应选用下列C装置收集.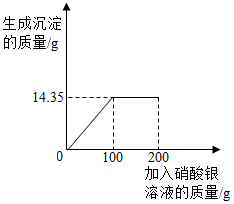 钠元素在人体内可起到调节体液平衡,维持肌肉正常兴奋和细胞的通透性等作用.假设钠元素全部来源于食盐(NaCl).
钠元素在人体内可起到调节体液平衡,维持肌肉正常兴奋和细胞的通透性等作用.假设钠元素全部来源于食盐(NaCl).