题目内容
4.物质是由分子、原子、离子构成的.请各举一例:由分子构成的物质如水;由原子构成的物质如铁;由离子构成的物质如氯化钠.世界上的物质是由一百余种元素组成的,如水是由氢元素和氧元素组成的.分析 根据金属、大多数固态非金属单质、稀有气体等由原子构成;有些物质是由分子构成的,气态的非金属单质和由非金属元素组成的化合物,如氢气、水等;有些物质是由离子构成的,一般是含有金属元素和非金属元素的化合物,如氯化钠,水是由氢元素和氧元素组成的,进行分析解答即可.
解答 解:分子,原子和离子都是构成物质的粒子;有的物质由分子构成,如水、二氧化碳、氧气等;有的物质由原子构成,如铜(属于金属单质,是由铜原子直接构成的)等(合理即可);有的物质由离子构成,如氯化钠(是由钠离子和氯离子构成的)等.水是由氢元素和氧元素组成的.
故答案为:水; 铁; 氯化钠; 氢元素和氧元素.
点评 本题难度不大,主要考查了构成物质的微观粒子方面的知识,对物质进行分类与对号入座、掌握常见物质的粒子构成是正确解答本题的关键.

练习册系列答案
相关题目
15.在元素周期表中,你发现元素种类最多的是( )
| A. | 金属 | B. | 非金属 | C. | 稀有气体 | D. | 不能确定 |
12.(1)一个铁原子的质量是M千克,一个碳-12原子的质量是N千克,列算式求出铁原子的相对原子质量
(2)完成下列表格
(2)完成下列表格
| 原子种类 | 质子数 | 中子数 | 电子数 | 相对原子质量(Ar) |
| 氮 | 7 | 7 | 7 | 14 |
| 钾 | 19 | 20 | 19 | 39 |
| 汞 | 80 | 121 | 80 | 201 |
19.铁、铝、铜是常见的三种金属.同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理.
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格.将粗细相同的铁丝、铝丝、铜丝分别插入体积相同、溶质质量分数也相同的稀盐酸中:
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面的氧化物会先与盐酸反应.
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是除去表面的氧化物.
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
写出铁与硫酸铜溶液反应的化学方程式Fe+CuSO4═FeSO4+Cu.
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序.金属丝的插入顺序为铜丝,铁丝和铝丝.
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序铜、铁、铝.
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格.将粗细相同的铁丝、铝丝、铜丝分别插入体积相同、溶质质量分数也相同的稀盐酸中:
| 操作 | 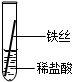 | 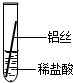 | 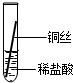 | 根据现象得出金属活动性顺序 |
| 片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al,Fe>Cu |
| 几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 | Al>Fe>Cu |
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是除去表面的氧化物.
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
| 操作 |  | 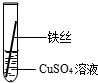 | 根据现象得出金属活动性顺序 |
| 现象 | 无明显现象 | 铁丝表面附着了一层红色固体 | Al>Fe>Cu |
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序.金属丝的插入顺序为铜丝,铁丝和铝丝.
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序铜、铁、铝.
9.某市对初中毕业生进行了化学实验操作考查.老师为同学们提供了几种无标签的固体和液体,要求对固体和液体的反应进行探究.
小明同学从一瓶固体和一瓶液体中各取少量于试管中进行混合,立即产生一种无色气体.该气体是什么物质,小明提出了自己的猜想.
(1)请你帮助他完成下列探究报告.
(2)现提供以下实验装置,要制取猜想的气体,依据的化学反应的原理是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑(用化学方程式表示).你选择的发生装置和收集装置分别是B 和C或D(填装置序号).
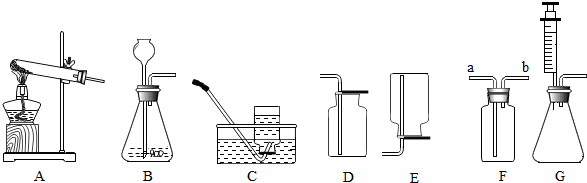
(3)如果用图F装置收集该气体(排空气法),该气体应由a(填“a”或“b”)端进入.
(4)如果用图G装置代替上述B装置制取气体,相比之下,该装置的优点是(写出两点)可控制化学反应的速率,可控制液体药品的用量.
(5)此无色气体还有可能是另外一种气体,写出产生它的化学方程式是CaCO3+2HCl=CaCl2+CO2↑+H2O.
小明同学从一瓶固体和一瓶液体中各取少量于试管中进行混合,立即产生一种无色气体.该气体是什么物质,小明提出了自己的猜想.
(1)请你帮助他完成下列探究报告.
| 猜想与假设 | 操作方法 | 证明猜想正确的实验现象 |

(3)如果用图F装置收集该气体(排空气法),该气体应由a(填“a”或“b”)端进入.
(4)如果用图G装置代替上述B装置制取气体,相比之下,该装置的优点是(写出两点)可控制化学反应的速率,可控制液体药品的用量.
(5)此无色气体还有可能是另外一种气体,写出产生它的化学方程式是CaCO3+2HCl=CaCl2+CO2↑+H2O.
13.为除去下列物质中的杂质(括号内为杂质),下列操作方法不能达到目的是( )
| 选项 | 物质(杂质) | 操作方式 |
| A | Fe(Cu) | 加足量稀硫酸,充分反应后过滤 |
| B | NaOH溶液(Ca(OH)2) | 加入适量的Na2CO3,充分反应后过滤 |
| C | NaCl溶液(Na2CO3) | 加入过量盐酸 |
| D | Fe2(SO4)3溶液(CuSO4) | 加入足量铁屑,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
 大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,分别开展以下探究:
大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,分别开展以下探究: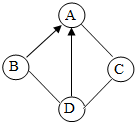 A、B、C、D是初中教材中常见的物质,相互间的关系右下图所示(“→”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应).通常情况下A是能参与绿色植物光合作用的气体;B是氧化铜,C、D的浓溶液有强烈的腐蚀性.
A、B、C、D是初中教材中常见的物质,相互间的关系右下图所示(“→”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应).通常情况下A是能参与绿色植物光合作用的气体;B是氧化铜,C、D的浓溶液有强烈的腐蚀性.