题目内容
如图(1)为甲、乙(均不含结晶水)两种固体物质的溶解度曲线.
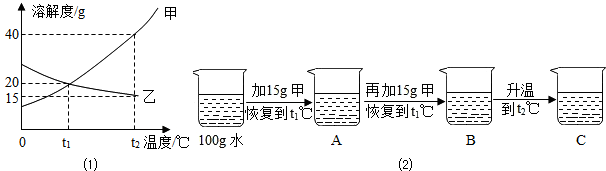
①t1℃时,甲的溶解度 (填“大于”“小于”或“等于”)乙的溶解度;若要从甲的饱和溶液中得到固体甲,则采用 方法.
②某同学在t1℃时开始进行如图(2)实验,在烧杯A、B、C中能得到饱和溶液的是 (填编号),溶质质量分数最大的是 (填编号);
③烧杯C中再加入15g甲后,充分搅拌,恢复到t2℃时,所得溶液的质量是 g.

①t1℃时,甲的溶解度
②某同学在t1℃时开始进行如图(2)实验,在烧杯A、B、C中能得到饱和溶液的是
③烧杯C中再加入15g甲后,充分搅拌,恢复到t2℃时,所得溶液的质量是
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,饱和溶液和不饱和溶液
专题:溶液、浊液与溶解度
分析:①根据曲线中交点的含义和固体物质从溶液中结晶析出的方法考虑;②根据t1℃时甲物质的溶解度为20g以及t2℃时甲物质的溶解度为40g进行解答;
解答:解:①曲线中交点表示该温度时两种物质的溶解度相等,所以t1℃时,甲的溶解度等于乙的溶解度;如果溶解度受温度影响较大的物质从溶液中结晶析出的方法是冷却热饱和溶液,如果溶解度受温度影响不大的物质从溶液中结晶析出的方法是蒸发溶剂.甲的溶解度受温度影响较大,所以用冷却热的饱和溶液的方法得到甲固体;
②t1℃时甲物质的溶解度为20g,所以t1℃时100g水中溶解15g甲物质,为不饱和溶液;再加入15g甲物质,只能再溶解5g,所以溶液是饱和溶液;t2℃时甲物质的溶解度为40g,所以升温后变为不饱和溶液,由于A中溶解了15g溶质,B中溶解了20g溶质,C中溶解了30g溶质,所以溶液溶质质量分数最大的是C.
③t2℃时甲物质的溶解度为40g,烧杯C中再加入15g甲后,溶质共45g,只能溶解40g,所以所得溶液质量为:40g+100g=140g.
故答案为:①等于;冷却热饱和溶液;②B;C;③140.
②t1℃时甲物质的溶解度为20g,所以t1℃时100g水中溶解15g甲物质,为不饱和溶液;再加入15g甲物质,只能再溶解5g,所以溶液是饱和溶液;t2℃时甲物质的溶解度为40g,所以升温后变为不饱和溶液,由于A中溶解了15g溶质,B中溶解了20g溶质,C中溶解了30g溶质,所以溶液溶质质量分数最大的是C.
③t2℃时甲物质的溶解度为40g,烧杯C中再加入15g甲后,溶质共45g,只能溶解40g,所以所得溶液质量为:40g+100g=140g.
故答案为:①等于;冷却热饱和溶液;②B;C;③140.
点评:解答本题关键是要知道溶解度曲线的意义,交点的含义,溶质结晶析出的方法,溶质质量的分数的计算方法,没溶解的不能计算在内.

练习册系列答案
相关题目
化学用语是世界通用的化学语言.有关物质的化学符号书写正确的是( )
| A、氯化铁:FeCl2 |
| B、氧化铝:Al2O3 |
| C、水银:Ag |
| D、二氧化硫:SiO2 |
二溴海因(化学式为:C5H6O2N2Br2)是一种广谱高效、低残留的新型环境消毒剂,关于二溴海因说法正确的是( )
| A、二溴海因的摩尔质量为286 g |
| B、1摩尔二溴海因中含6.02×1023个N2分子 |
| C、二溴海因中氧元素的质量分数小于氮元素的质量分数 |
| D、1摩尔二溴海因中C、H、O、N、Br原子个数比为5:6:2:2:2 |
比较是化学学习常用的方法,下列各物质的比较正确的是( )
| A、氧气和二氧化碳都含氧元素,二者都是氧化物 |
| B、铁在空气中易锈蚀,而铝很耐腐蚀,说明铁比铝活泼 |
| C、乙醇和甲烷都含碳元素,二者都是有机物 |
| D、氧化钙和浓硫酸分别加入水都放热,都是发生化学变化 |



 A、B、C、D都是初中化学中常见物质,A是人类赖以生存的一种无色液体,D是一种黑色固体,具有如图所示的转化关系(反应条件、其他反应物及多余产物均略去):
A、B、C、D都是初中化学中常见物质,A是人类赖以生存的一种无色液体,D是一种黑色固体,具有如图所示的转化关系(反应条件、其他反应物及多余产物均略去):