题目内容
2009年2月某市发生的“瘦肉精”中毒事件造成几十人住院治疗.“瘦肉精”(化学式为C12H19Cl3N2O)能提高猪的瘦肉率,但对人体有危害,我国多年前已经禁止使用.请回答:(1)“瘦肉精”由______种元素组成,其分子中氢、氧原子的个数比为______.
(2)“瘦肉精”的相对分子质量为______.
(3)“瘦肉精”中______元素的质量分数最大,为______.
(4)多少克“瘦肉精”中含有56克氮元素,同时含有多少克氯元素?
【答案】分析:(1)根据化学式可知道物质的元素组成以及分子中各原子的个数比;
(2)化学式中各原子的相对原子质量的总和,就是相对分子质量;
(3)根据质量分数的公式:某元素的质量分数= ×100%计算即可;
×100%计算即可;
(4)化合物中某一元素的质量=该物质的质量×该元素的质量分数.
解答:解:(1))根据“瘦肉精”化学式为C12H19Cl3N2O,可知“瘦肉精”由C、H、Cl、N、O五种元素组成,一个“瘦肉精”分子中有19个氢原子、1个氧原子,氢、氧原子的个数比为 19:1;
(2)瘦肉精C12H19Cl3N2O的相对分子质量为12×12+1×18+35.5×3+14×2+16=313.5;
(3)物质中某元素的质量分数= ×100%计,通过比较可知碳 元素的质量分数最大,瘦肉精中碳元素的质量分数是
×100%计,通过比较可知碳 元素的质量分数最大,瘦肉精中碳元素的质量分数是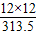 ×100%≈45.9%;
×100%≈45.9%;
(4)设质量为x的“瘦肉精”中含有56克氮元素,则x×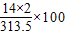 %=56g
%=56g
解得x=627g.
同时含有氯元素的质量为627g×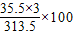 %=213g.
%=213g.
故答案为:(1)五;19:1;
(2)313.5;
(3)碳;45.9%;
(4)627g;213g.
点评:主要考查了相对分子质量的计算方法、元素质量分数的求法以及利用相对质量求物质中所含元素的比值的方法,这些基本计算要求掌握.
(2)化学式中各原子的相对原子质量的总和,就是相对分子质量;
(3)根据质量分数的公式:某元素的质量分数=
 ×100%计算即可;
×100%计算即可;(4)化合物中某一元素的质量=该物质的质量×该元素的质量分数.
解答:解:(1))根据“瘦肉精”化学式为C12H19Cl3N2O,可知“瘦肉精”由C、H、Cl、N、O五种元素组成,一个“瘦肉精”分子中有19个氢原子、1个氧原子,氢、氧原子的个数比为 19:1;
(2)瘦肉精C12H19Cl3N2O的相对分子质量为12×12+1×18+35.5×3+14×2+16=313.5;
(3)物质中某元素的质量分数=
 ×100%计,通过比较可知碳 元素的质量分数最大,瘦肉精中碳元素的质量分数是
×100%计,通过比较可知碳 元素的质量分数最大,瘦肉精中碳元素的质量分数是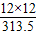 ×100%≈45.9%;
×100%≈45.9%;(4)设质量为x的“瘦肉精”中含有56克氮元素,则x×
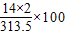 %=56g
%=56g 解得x=627g.
同时含有氯元素的质量为627g×
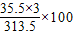 %=213g.
%=213g.故答案为:(1)五;19:1;
(2)313.5;
(3)碳;45.9%;
(4)627g;213g.
点评:主要考查了相对分子质量的计算方法、元素质量分数的求法以及利用相对质量求物质中所含元素的比值的方法,这些基本计算要求掌握.

练习册系列答案
相关题目