题目内容
16. 某化学兴趣小组对一包干燥的红色粉末组成进行探究,同学们根据该红色粉末的来源,判断其可能由Cu、Fe2O3两种固体中的一种或两种组成.
某化学兴趣小组对一包干燥的红色粉末组成进行探究,同学们根据该红色粉末的来源,判断其可能由Cu、Fe2O3两种固体中的一种或两种组成.Ⅰ.定性探究:
【提出猜想】该红色粉末可能是:①Cu ②Fe2O3 ③Cu和Fe2O3
【查阅资料】Cu在FeCl3溶液中发生反应:2FeCl3+Cu═2FeCl2+CuCl2
【设计实验】(1)小玲取少量红色粉末于试管中,滴加足量稀盐酸,充分振荡后观察,发现固体全部溶解,得有色溶液.则猜想①一定不成立.
(2)小伟向小玲得到的有色溶液中插入一根洁净的铁丝,反应充分后,观察到铁丝表面有一层红色物质析出现象,得出猜想③成立.
Ⅱ.定量探究:
【提出问题】该红色粉末中氧化铁的质量分数是多少呢?
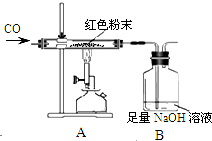
【设计实验】小晨称取该红色粉末5.0g装入硬质玻璃管中,按如图进行实验,开始时缓缓通入CO气体,过一段时间后再加热至高温使其充分反应,待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却,反应前后称量相关物质的总质量(装置内空气中的水蒸气、CO2忽略不计),其数据如表:
| 反应前 | 反应后 | |
| Ⅰ组 | 玻璃管和红色粉末的总质量为48.3g | 玻璃管和固体物质的总质量为47.1g |
| Ⅱ组 | 洗气瓶和瓶中所盛物质的总质量为258.6g | 洗气瓶和瓶中所盛物质的总质量为261.9g |
(1)在装置A中先通CO气体的目的是排尽空气,防止爆炸,A装置中发生反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)为了防止溶液倒吸,本实验最后停止加热前是否需要先断开装置中A和B的连接处?不需要(填“需要”或“不需要”),理由是实验中持续通入一氧化碳气体直到玻璃管内物质冷却.
(3)从环保的角度分析,该装置的缺陷是缺少尾气处理装置.
(4)根据上述表格中的实验数据计算:红色粉末中氧化铁的质量分数为80%.
分析 由题目给出的信息可知:取少量红色粉末于试管中,滴加足量稀盐酸,充分振荡后观察,发现固体全部溶解,得有色溶液;则猜想①一定不成立,因为铜与盐酸不反应;小伟向小玲得到的有色溶液中插入一根洁净的铁丝,反应充分后,观察到铁丝表面有红色物质生成,得出猜想③成立;在装置A中先通CO气体的目的是:排尽玻璃管内空气;根据上述表格中的实验数据计算:氧元素的质量=48.3g-47.1g=1.2g,氧化铁的质量=1.2g÷$\frac{48}{160}$=4g;红色粉末中氧化铁的质量分数=$\frac{4g}{5g}$×100%=80%;本装置的不足之处是:没有尾气处理装置,改进方法是:在B装置的导管口点燃一氧化碳或扎一个气球.
解答 解:【设计实验】(1)取少量红色粉末于试管中,滴加足量稀盐酸,充分振荡后观察,发现固体全部溶解,得有色溶液;则猜想①一定不成立,因为铜与盐酸不反应;故填:①;
(2)小伟向小玲得到的有色溶液中插入一根洁净的铁丝,反应充分后,观察到铁丝表面有红色物质生成,得出猜想③成立;故填:铁丝表面有一层红色物质析出
;
【交流讨论】
(1)在装置A中先通CO气体的目的是 排出玻璃管内的空气,B装置的作用是 吸收反应产生的CO2.一氧化碳能与氧化铁高温反应生成铁和二氧化碳,故填:排尽空气,防止爆炸;3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)因为实验结束后是持续通入一氧化碳知道玻璃管冷却,故不需要先断开装置中A和B的连接处,故填:不需要;实验中持续通入一氧化碳气体直到玻璃管内物质冷却;
(3)从环保角度看上述装置有严重不足之处是:没有尾气处理装置,改进方法是:在B装置的导管口点燃一氧化碳或扎一个气球;故填:缺少尾气处理装置;
(4)根据上述表格中的实验数据计算:氧元素的质量=48.3g-47.1g=1.2g,氧化铁的质量=1.2g÷$\frac{48}{160}$=4g;红色粉末中氧化铁的质量分数=$\frac{4g}{5g}$×100%=80%;故填:80%.
点评 实验探究题是近几年中考的重点内容之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过查阅资料和实验分析,得到了正确的结论,属于结论性探究,有关的计算要准确.同学们要具体分析,综合掌握,本考点主要出现在实验题中.

| A. | ①③⑤ | B. | ③④⑤ | C. | ①②④⑤ | D. | ①②③④⑤ |
| A. | 复分解 | B. | 还原 | C. | 分子 | D. | 加成 |
| 物 质 | A | B | C | D |
| 反应前质量/g | 19.7 | 8.7 | 21.6 | 0.4 |
| 反应后质量/g | 待测 | 17.4 | 0 | 3.6 |
| A. | 物质C一定是化合物,物质D可能是单质 | |
| B. | 反应后密闭容器中A的质量为19.7g | |
| C. | 反应过程中,物质B和物质D变化的质量比为87:36 | |
| D. | 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为2:1 |

请分析实验过程,回答下列问题:
(1)白色粉末中一定不含CuSO4、Na2SO4;可能含有NaOH.
(2)生成白色沉淀的化学方程式为Na2CO3+BaCl2=BaCO3↓+2NaCl.
(3)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究.
【提出问题】无色滤液中呈碱性的物质是什么?
【作出猜想】猜想Ⅰ:Na2CO3
猜想Ⅱ:NaOH
猜想Ⅲ:Na2CO3和NaOH
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取无色滤液少许于试管中,滴加BaCl2溶液 | 产生白色沉淀 | 猜想Ⅱ不成立 |
| ②在①反应后的试管中滴加无色酚酞溶液 | 溶液变为红色 | 猜想Ⅲ成立 |
(1)鸭蛋中富含的营养素有水和蛋白质.
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是生石灰与水反应放出大量的热.
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为红色.
同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中除含有NaOH和NaCl外,还含有那些溶质?
【猜想】甲同学推断只有Ca(OH)2;
乙同学推断只有Na2CO3;
丙同学推断有Ca(OH)2、也有Na2CO3;
通过进一步讨论,大家一致认为丙同学的猜想是错误的,其他两个还需探究.
【实验探究】
| 实验步骤 | 实验现象 |
| ①取少量上层料液,滴加稀盐酸 | 无明显现象 |
| ②另取少量上层料液,滴加碳酸钠溶液 | 产生白色沉淀 |
【问题与思考】
(1)实验①加入足量稀盐酸的目的是检验料液中是否含有碳酸钠.
(2)新做的皮蛋往往带有涩味,食用时可以加入适量的食醋.
已知:MgO+2HCl=MgCl2+H2O
MgCO3+2HCl=MgCl2+H2O+CO2↑
(1)探究“镁粉”中是否含有Mg和MgCO3
(2)①取少量样品,如图1所示进行实验.观察到a试管中有气泡产生,b试管中产生的现象是澄清石灰水变浑浊,则证明“镁粉”中一定含有MgCO3.
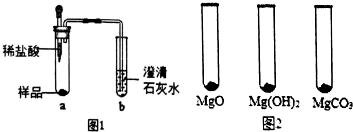
②为证明“镁粉”中是否含有Mg,小明将燃着的木条放在图中b试管口上方,木条熄灭.但同学们指出,该实验不能达成实验目的,需要将图中的澄清石灰水替换成浓NaOH溶液,目的是把二氧化碳全部吸收.小明按照修改后的实验方案重复上述实验,观察到b试管口无明显现象,证明“镁粉”中没有Mg.
(3)探究“镁粉”中是否还含有MgO及Mg(OH)2
【实验过程】
Ⅰ.用MgO、Mg(OH)2和MgCO3三种固体分别做性质实验.分别取0.5g三种固体粉末,每次取样方法如图2所示:
逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失.在下表中记录消耗的同浓度稀盐酸的体积(以下体积均在同一条件下测定,且保留到小数点后1位)
| MgO | Mg(OH)2 | MgCO3 | |
| 消耗稀盐酸的体积/mL | 10.4 | 7.2 | 5.0 |
Ⅱ.取“镁粉”样品0.5g,加入上述稀盐酸至粉末恰好溶解.此时消耗稀盐酸的体积约为5.3mL.
【实验分析及结论】
“镁粉”不只含有MgCO3.理由是0.5g“镁粉”消耗稀盐酸的体积与0.5gMgCO3消耗稀盐酸的体积不相等.
【实验反思】
为确定“镁粉”的具体成分,同学们认为还需要补充如下实验:分别取0.5g“镁粉”和0.5gMgCO3,加入足量稀盐酸,测定生成的气体体积分别为119mL和140mL.由此可知“镁粉”中含有MgCO3的质量分数为85%.
| A. | H2 | B. | H2SO4 | C. | 2C | D. | C2H2 |