题目内容
2.如表是KNO3和NaCl在不同温度下的溶解度,请回答下列问题:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 /g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 35.7 | 36 | 36.6 | 37.3 | 38.4 | 39.8 | |
(2)20℃时,将KNO3不饱和的溶液,转化成该温度下的饱和溶液的一种方法是继续加KNO3至不再溶解;
(3)欲配制一定量的KNO3浓溶液以备稀释使用,你认为40℃时,不能(填“能”或“不能”)配制出63.9%的KNO3溶液.
(4)80℃时,把113.3g KNO3和20gNaCl全部放入100g水中,充分溶解后将溶液降温至0℃时,溶液中NaCl的质量是20g,析出KNO3的质量是100g. 由此得出从KNO3和NaCl的混合溶液中提纯KNO3的方法是降温结晶.
分析 (1)根据KNO3和NaCl在不同温度下的溶解度分析回答;
(2)根据不饱和的溶液和饱和溶液之间的转化分析回答;
(3)根据40℃时,KNO3的溶解度计算分析;
(4)根据溶解度的意义计算、分析判断.
解答 解:(1)40℃时,NaCl的溶解度是36.6g,从表中数据可以看出影响物质溶解度的因素是温度;
(2)20℃时,将KNO3不饱和的溶液,转化成该温度下的饱和溶液的一种方法是继续加KNO3至不再溶解;
(3)由表中的数据可知,在40℃时KNO3溶解度是63.9g,所形成的饱和溶液的质量分数是:$\frac{63.9g}{100g+63.9g}×100%$≈39%,所以不能配制出63.9%的溶液.
(4)由于在60℃时,KNO3的溶解度是110g,NaCl的溶解度是37.3g,在0℃时,KNO3的溶解度是13.3g,NaCl的溶解度是35.7g所以,60℃时,把113.3g KNO3和20g NaCl全部放入100g水中,充分溶解后形成KNO3和NaCl的不饱和溶液,溶液中NaCl的质量是20g,0℃时,溶液中NaCl的质量是20g,析出KNO3的质量是100g.由此得出从KNO3和NaCl的混合溶液中KNO3提纯的方法是降温结晶.
故答为:(1)36.6g,温度;(2)继续加KNO3至不再溶解;(3)不能;(4)20,100,降温结晶.
点评 此题是溶解度知识的具体应用,对学生深入理解溶解度的概念有一定帮助,同时也复习了有关混合物分离的一些常识性的基础知识.

练习册系列答案
相关题目
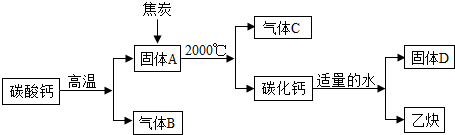
12.电石,学名碳化钙(CaC2),以焦炭和碳酸钙为原料生产碳化钙并制备重要工业原料乙炔(CxHy)气体的原理如下图.
【实验探究】
(1)C与B的组成元素相同,有毒,写出固体A和焦炭反应得到碳化钙的化学方程式为CaO+3C$\frac{\underline{\;高温\;}}{\;}$CaC2+CO↑.
(2)小组同学对D提出三种猜想:猜想一:氧化钙;猜想二:氢氧化钙;猜想三:碳酸钙.同学们经过分析将猜想一排除,理由是氧化钙与水反应生成氢氧化钙.
(3)验证该固体D:取样,滴加稀盐酸,观察到固体溶解,无气泡产生,猜想二正确.
【组成测定】
(一)实验设计:
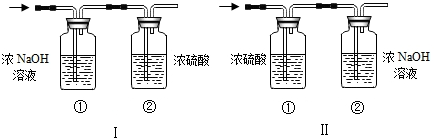
将一定量的乙炔(CxHy)完全燃烧,生成的气体全部缓缓通过下图II装置(选填Ⅰ或Ⅱ).
(二)实验测定:
小资料:一个乙炔分子中共有四个原子构成
实验数据记录数据于下表中,试通过计算,确定乙炔的化学式.
计算过程:
结论:乙炔的化学式C2H2
【归纳小结】写出碳化钙与水反应的化学方程CaC2+2H2O=Ca(OH)2+C2H2↑.

【实验探究】
(1)C与B的组成元素相同,有毒,写出固体A和焦炭反应得到碳化钙的化学方程式为CaO+3C$\frac{\underline{\;高温\;}}{\;}$CaC2+CO↑.
(2)小组同学对D提出三种猜想:猜想一:氧化钙;猜想二:氢氧化钙;猜想三:碳酸钙.同学们经过分析将猜想一排除,理由是氧化钙与水反应生成氢氧化钙.
(3)验证该固体D:取样,滴加稀盐酸,观察到固体溶解,无气泡产生,猜想二正确.
【组成测定】
(一)实验设计:
将一定量的乙炔(CxHy)完全燃烧,生成的气体全部缓缓通过下图II装置(选填Ⅰ或Ⅱ).

(二)实验测定:
小资料:一个乙炔分子中共有四个原子构成
实验数据记录数据于下表中,试通过计算,确定乙炔的化学式.
计算过程:
| 反应前质量/g | 反应后质量/g | |
| 装置① | 125.3 | 127.1 |
| 装置② | 78.2 | 87.0 |
【归纳小结】写出碳化钙与水反应的化学方程CaC2+2H2O=Ca(OH)2+C2H2↑.
17.下列关于金属材料的说法正确的是( )
| A. | 铝、铁、铜都是银白色 | B. | 沙漠地区的铁制品锈蚀较快 | ||
| C. | 铝土矿的主要成分是Al2O3 | D. | 生铁是纯金属,钢是铁的合金 |
11.对下列物质:①红磷②木炭③铁丝④硫分别在氧气中燃烧的描述,正确的是( )
| A. | 剧烈燃烧、发出耀眼白光的是铁 | |
| B. | 产生蓝紫色火焰的是硫 | |
| C. | 有能使澄清石灰水变浑浊的白色气体产生的是木炭 | |
| D. | 有白色且有刺激性气味气体生成的是红磷 |
 人类的日常生活和工农业生产离不开水.请回答:
人类的日常生活和工农业生产离不开水.请回答: