题目内容
7.在一定温度下,将36g硝酸钾完全溶于204g 水中,将所得的溶液分为二等份,计算:①每一份溶液中溶质的质量分数
②取第一份溶液,要使其溶质的质量分数比原来增加一倍,可以蒸发掉多少水;
③取第二份溶液向其中再加入7.5g 硝酸钾完全溶解后,所得溶液中溶质的质量分数是多少?
分析 根据溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%,若想求溶液中溶质的质量分数只要找出相应的溶质的质量和溶液的质量即可.
解答 解:将36g硝酸钾完全溶于204g 水中,所得溶液中溶质的质量分数为$\frac{36g}{36g+204g}$×100%=15%.
①由于溶液具有均一性,将所得溶液平均分成二等份,其中每一份溶液的溶质的质量分数均是15%.
②取第二份,要使其溶质的质量分数比原来增加一倍,即溶液中溶质的质量分数变成30%,可设可以蒸发掉水的质量为x.
30%=$\frac{36g}{36g+204g-x}$×100%,x=60g;
答:可以蒸发掉60g水;
③$\frac{18g+7.5g}{18g+7.5g+102g}$×100%=20%.
答:所得溶液中溶质的质量分数是20%.
点评 本题难度不是很大,主要考查了有关溶液中溶质质量分数的简单计算,从而加深学生对溶质质量分数概念的理解,培养学生的计算能力和理解能力.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
18.有下列五种物质,①汽车排气所形成的烟雾;②石油化工厂排放的废气;③天然水蒸发成水蒸气;④植物进行光合作用所放出的气体;⑤煤燃烧产生的烟尘,其屮能严重污染空气、对人类适成很大危害的物质是( )
| A. | 只有③④ | B. | 只有①②⑤ | C. | 只有③⑤ | D. | 只有①③④ |
15.下列实验操作正确的是( )
| A. | 用剩的试剂一定要放回原处 | B. | 可用嘴尝任何试剂的味道 | ||
| C. | 垫上石棉网给烧杯内的液体加热 | D. | 把鼻子凑到试剂瓶口闻气味 |
2.从化学的角度看,下列说法错误的是( )
| A. | “风吹桂花满院香”,说明微粒是不断运动的 | |
| B. | 铁在潮湿的空气中易生锈,表面喷漆可以防锈 | |
| C. | 正在使用的家用电器着火时,应立即关闭开关 | |
| D. | 因为氧气能支持燃烧,所以可用作燃料 |
17.如图所示的实验操作中正确的是( )
| A. | 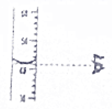 量取液体 | B. | 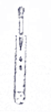 滴加液体 | C. | 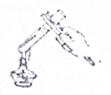 加热液体 | D. |  点燃酒精灯 |