题目内容
某兴趣小组用10g镁条与一定溶质质量分数的稀硫酸反应,测得产生氢气的质量与稀硫酸的质量关系如图所示(假设镁条中除表面含有氧化镁外,没有其他杂质)
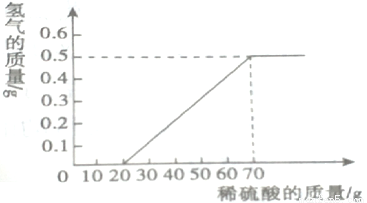
(1)当所用稀硫酸的质量为70g,产生的氢气的质量为__________.。
(2)用化学方程式说明当稀硫酸的质量为10g时,为什么不产生氢气:___________。
(3)计算稀硫酸中溶质的质量分数____________?
0.5g MgO + H2SO4 ===MgSO4 + H2O 49% 【解析】(1)由图可知,当所用稀硫酸的质量为70g,产生的氢气的质量为0.5g; (2)当稀硫酸的质量为10g时,稀硫酸与镁表面的氧化镁反应,生成氯化镁和水, 反应方程式为MgO + H2SO4 ===MgSO4 + H2O; (3)设生成0.5g的氢气需要硫酸的质量为x Mg + H2SO4 ===M...
练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
某密闭容器中有甲、乙、丙、丁四种物质,一定条件充分反应后,实验数据如下表。下列说法错误的是
甲 | 乙 | 丙 | 丁 | |
反应前质量/g | 18 | 4 | 19 | 20 |
反应后质量/g | 2 | 待测 | 29 | 26 |
A. 乙在该反应中可能是催化剂 B. 该反应属于化合反应
C. 甲、丙在反应中的质量比为8︰5 D. 该反应遵守质量守恒定律
B 【解析】根据质量守恒定律求出待测为18+4+19+20-26-29-2=4;根据反应过程中质量的变化确定甲为反应物,丙、丁为生成物,乙可能为催化剂也可能不起任何作用;根据反应工程中的质量变化求得甲、丙的质量比。 A. 乙在该反应中可能是催化剂,正确; B.由表中数据可知,该反应为分解反应,故错误; C. 在反应过程中甲的质量变化为16g,丙的质量变化为10g ,因此甲、...