题目内容
15.向一定量4%的氢氧化钠溶液中逐滴加入稀盐酸,有关分析错误的是( )| A. |  | B. | 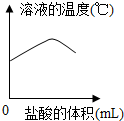 | C. | 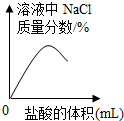 | D. |  |
分析 解答本题可首先分析图象所涉及的化学反应的实质,其次分析图象的起点和终点是否正确,最后分析图象的变化趋势是否合题意即可.
解答 解:A.开始时氢氧化钠溶液是碱性,pH大于7,随着稀盐酸的滴加,pH逐渐减小,但稀盐酸过量时pH小于7,所以图象正确;
B.酸碱中和反应会放出热量,故随着稀盐酸的加入,溶液的温度升高,当恰好完全中和时,溶液温度最高,继续滴加稀盐酸,溶液的温度就会降低,所以图象正确;
C.没有滴加稀盐酸时,溶液中氯化钠的质量分数为零,随着加入稀盐酸生成的氯化钠越来越多,溶液中氯化钠的质量分数越来越大,当二者完全中和时,溶液中氯化钠的质量分数达到最大值且不再增加,再滴加稀盐酸,溶液的质量增大,氯化钠的质量不变,溶液中氯化钠的质量分数减小,故图象正确;
D.当加入的稀盐酸与氢氧化钠发生反应时,HCl的物质的量为零,当二者恰好完全反应时,继续滴加稀盐酸,HCl的物质的量增加,且随着稀盐酸加入的量的增多,而不断增大,故图象错误.
故选D.
点评 本题是化学反应中定量关系和图象相结合的题型,题目难度较大;要准确解答此类题,关键要对化学反应知识熟练,并能结合图象的数学意义,综合考虑,可快速解答;图象的意义要抓住三点:①抓图象的起点,②抓图象的终点,③抓图象的变化过程.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
6.下列说法中,不正确的是( )
| A. | 如果不加入催化剂,过氧化氢就不会分解 | |
| B. | 自然界中的物质都在不断运动 | |
| C. | 增大氧气的浓度能促进可燃物的燃烧 | |
| D. | 任何纯净物都有固定的组成 |
10.互为同素异形体的一组物质是( )
| A. | 金刚石、石墨 | B. | 双氧水、水 | C. | 干冰、冰 | D. | 氧气、液氧 |
20.学校常用福尔马林(40%甲醛溶液)来浸制标本,已知甲醛的化学式是CH2O,关于甲醛的说法错误的是( )
| A. | 是一种有机物 | B. | 由碳、氢、氧元素组成 | ||
| C. | 碳、氢、氧元素的质量比是1:2:1 | D. | 相对分子质量为30 |
7.用已知溶质质量分数的溶液可以测定未知溶液的质量分数,实验室有一瓶标签模糊的稀盐酸,某同学为了测定其溶质质量分数,进行了如下实验.
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量);
②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量,数据如下表:
(1)若要配制500克16%的氢氧化钠溶液,需要氢氧化钠固体80克;
(2)本次实验中,实际消耗的氢氧化钠溶液质量为25克;
(3)请通过计算确定该瓶稀盐酸的溶质质量分数;
(4)另有同学做了同样实验,却得到了不同的结果,于是用精密pH试纸测得反应后锥形瓶内溶液的pH为8.2,则他测出的盐酸溶质质量分数偏大(选填“偏大”或“偏小”),造成这一偏差的原因是滴加的氢氧化钠溶液过量.
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量);
②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量,数据如下表:
| 锥形瓶 | 锥形瓶+稀盐酸 | 锥形瓶+反应后溶液 | |
| 质量(克) | 35.5 | 55.5 | 80.5 |
(2)本次实验中,实际消耗的氢氧化钠溶液质量为25克;
(3)请通过计算确定该瓶稀盐酸的溶质质量分数;
(4)另有同学做了同样实验,却得到了不同的结果,于是用精密pH试纸测得反应后锥形瓶内溶液的pH为8.2,则他测出的盐酸溶质质量分数偏大(选填“偏大”或“偏小”),造成这一偏差的原因是滴加的氢氧化钠溶液过量.
17.下列课题侧重于化学学科研究领域的是( )
| A. | 计算机软件的开发 | |
| B. | “神七”飞船从地球轨道转到月球轨道 | |
| C. | 利用指南针确定航海方向 | |
| D. | 新型可降解塑料袋的研制 |
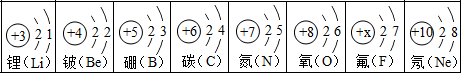
 ,图中与其化学性质相似的元素是氧.
,图中与其化学性质相似的元素是氧.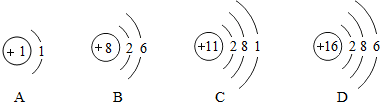
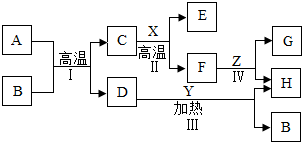 (1)X、Y、Z、W、R是初中化学常见的五种元素,X的单质是密度最小的气体,Y的一种单质是天然存在的最硬物质,Z是地壳中含量最多的元素,W的原子序数为11,R的原子结构示意图为
(1)X、Y、Z、W、R是初中化学常见的五种元素,X的单质是密度最小的气体,Y的一种单质是天然存在的最硬物质,Z是地壳中含量最多的元素,W的原子序数为11,R的原子结构示意图为 ,请回答下列问题:①X阳离子的离子结构示意图为
,请回答下列问题:①X阳离子的离子结构示意图为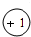 ,W离子的离子符号为Na+;
,W离子的离子符号为Na+;