题目内容
17.科学家采取“组合转化”技术,使CO2和H2发生反应,生成一种化工原料乙烯和水,化学方程式为:2CO2+6H2═乙烯+4H2O,则乙烯的化学式为( )| A. | C2H6 | B. | C2H4 | C. | C2H5OH | D. | C2H2 |
分析 根据质量守恒定律的实质可以知道,反应前后原子的种类不变,原子的个数不变,进行分析推断本题.
解答 解:根据质量守恒定律,反应物中总共有2个碳原子,4个氧原子和12个氢原子,而生成物中只有8个氢原子和4个原子,还少2个碳原子和4个氢原子,因此乙烯的化学式为C2H4.
故选B.
点评 根据反应的化学方程式,利用反应前后原子种类、数目不变,可推断反应中某物质的分子构成、确定该物质的化学式.

练习册系列答案
 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
7.单晶硅是制作集成电路的基础材料.工业上通过以下反应将自然界的二氧化硅(SiO2)转化为硅:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.下列分析正确的是( )
| A. | 碳发生了还原反应 | B. | 二氧化硅具有氧化性 | ||
| C. | 该反应属于分解反应 | D. | 反应前后固体质量不变 |
8.工业用盐亚硝酸钠(NaNO2),不能食用.亚硝酸钠中氮元素的化合价为( )
| A. | -3 | B. | +1 | C. | +3 | D. | +5 |
12.下列现象或事实,用分子、原子的相关知识加以解释,其中不正确是( )
| 现象或事实 | 解释 | |
| A | 稀有气体可作保护气 | 构成它们的原子达到了稳定结构 |
| B | 敞口容器中的酒精逐渐减少 | 分子在不断的运动 |
| C | 水沸腾后壶盖被顶起 | 温度升高,分子体积变大 |
| D | 水通电分解 | 在化学变化分子可以再分 |
| A. | A | B. | B | C. | C | D. | D |
2.鉴别日常生活中的下列各组物质,两种方法均正确的是( )
| A. | 硬水和软水:滴加食盐水或加热蒸发 | |
| B. | 食醋和酒精:闻气味或点燃观察现象 | |
| C. | 水和过氧化氢溶液:燃着的木条或加入二氧化锰 | |
| D. | 甲烷和一氧化碳:滴加澄清石灰水或观察燃烧火焰颜色 |
9.现代科技证明,葡萄酒中含有的白藜芦醇具有美容养颜之功效.下列关于白藜芦醇(C14H12O3)的说法正确的是( )
| A. | 白藜芦醇由是由14个碳原子、12个氢原子和3个氧原子构成 | |
| B. | 白藜芦醇中碳、氢、氧元素质量比为14:1 2:3 | |
| C. | 白藜芦醇是一种氧化物 | |
| D. | 白藜芦醇中中碳元素的质量分数约为73.7% |
6.下列有关燃烧的说法,正确的是( )
| A. | 能产生发光、放热现象的变化就是燃烧 | |
| B. | 同种物质完全燃烧和不完全燃烧,现象完全相同 | |
| C. | 只要温度达到着火点,可燃物就可以燃烧 | |
| D. | 发动机中的柴油以雾状喷出,有利于完全燃烧 |
7.下列不属于二氧化碳用途的是( )
| A. | 人工降雨 | B. | 灭火 | C. | 火箭燃料 | D. | 制碳酸饮料 |
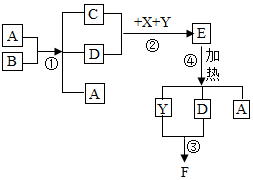 如图表示某些物质间的转化关系(部分反应条件省略).其中A为黑色固体氧化物;E为绿色固体;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y为常见无色气体;X是常见的红色金属单质.
如图表示某些物质间的转化关系(部分反应条件省略).其中A为黑色固体氧化物;E为绿色固体;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y为常见无色气体;X是常见的红色金属单质.