题目内容
10.在银杏果中含有银杏酸(银杏酸化学式为C22H34O3),下列有关银杏酸的说法正确的是( )| A. | 属于氧化物 | |
| B. | 碳、氢、氧三种元素质量比是22:34:3 | |
| C. | 氢元素的质量分数最大 | |
| D. | 由三种非金属元素组成 |
分析 A、氧化物是只含有两种元素且其中一种元素是氧元素的化合物.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D、根据碳、氢、氧三种元素的分类进行分析判断.
解答 解:A、银杏酸是由碳、氢、氧三种元素组成的化合物,不属于氧化物,故选项说法错误.
B、碳、氢、氧三种元素质量比是(12×22):(1×34):(16×3)≠22:34:3,故选项说法错误.
C、碳、氢、氧三种元素质量比是(12×22):(1×34):(16×3)=132:17:24,则碳元素的质量分数最大,故选项说法错误.
D、碳、氢、氧三种元素均为非金属元素,故选项说法正确.
故选:D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算等进行分析问题、解决问题的能力.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
18.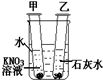 如图所示,在盛冷水烧杯中放入甲、乙两支试管(试管中都有未溶解的该溶液的溶质),若使甲试管中晶体减少,乙试管中晶体增加,需向烧杯中加入的物质是( )
如图所示,在盛冷水烧杯中放入甲、乙两支试管(试管中都有未溶解的该溶液的溶质),若使甲试管中晶体减少,乙试管中晶体增加,需向烧杯中加入的物质是( )
 如图所示,在盛冷水烧杯中放入甲、乙两支试管(试管中都有未溶解的该溶液的溶质),若使甲试管中晶体减少,乙试管中晶体增加,需向烧杯中加入的物质是( )
如图所示,在盛冷水烧杯中放入甲、乙两支试管(试管中都有未溶解的该溶液的溶质),若使甲试管中晶体减少,乙试管中晶体增加,需向烧杯中加入的物质是( )| A. | 氯化钠 | B. | 硝酸钾 | C. | 硝酸铵 | D. | 氢氧化钾 |
5.下列有关说法中错误的是( )
①原子一定比分子小
②最外层电子数为8的粒子一定是稀有气体元素的原子
③浓溶液一定是饱和溶液;稀溶液一定是不饱和溶液.
④同种元素在同一化合物中不一定显示一种化合价.
⑤单质也可以发生分解反应.
⑥凡金属与酸发生的置换反应,反应后溶液的质量一定增加.
①原子一定比分子小
②最外层电子数为8的粒子一定是稀有气体元素的原子
③浓溶液一定是饱和溶液;稀溶液一定是不饱和溶液.
④同种元素在同一化合物中不一定显示一种化合价.
⑤单质也可以发生分解反应.
⑥凡金属与酸发生的置换反应,反应后溶液的质量一定增加.
| A. | ①②④⑤ | B. | ①③④⑥ | C. | ①②③⑤ | D. | ①②③④⑤⑥ |
15.植物进行光合作用可表示为:水+二氧化碳 $→_{叶绿素}^{光}$ 淀粉+氧气,据此可知淀粉的组成一定含有的元素是( )
| A. | 碳、氢和氧 | B. | 碳、氧 | C. | 氢、氧 | D. | 碳、氢 |