题目内容
10.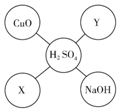 对知识的及时整理与归纳是学习科学的重要方法.某同学在学习了硫酸的化学性质后,初步归纳出稀硫酸与其他物质相互反应的关系,如图所示(“-”表示相连的两种物质能发生反应,五个圈中的物质属于不同的类别).
对知识的及时整理与归纳是学习科学的重要方法.某同学在学习了硫酸的化学性质后,初步归纳出稀硫酸与其他物质相互反应的关系,如图所示(“-”表示相连的两种物质能发生反应,五个圈中的物质属于不同的类别).(1)已知X是金属单质,则X可以是锌.(填一种即可)
(2)请写出稀硫酸与Y反应的一个化学方程式BaCl2+H2SO4═BaSO4↓+2HCl.
分析 (1)根据酸能与活泼金属反应,进行分析解答.
(2)根据酸的化学性质(能与活泼金属、金属氧化物、碱、碳酸盐等反应),据此进行分析解答.
解答 解:(1)酸能与活泼金属反应,已知X是金属单质,则X可以是锌、铁等金属.
(2)由题意,五个圈中的物质属于不同的类别,氧化铜属于金属氧化物,氢氧化钠属于碱,X为金属,则Y应为盐,硫酸能与氯化钡溶液反应生成硫酸钡沉淀和盐酸,反应的化学方程式为BaCl2+H2SO4═BaSO4↓+2HCl(合理即可).
故答案为:(1)锌;(2)BaCl2+H2SO4═BaSO4↓+2HCl(合理即可).
点评 本题难度不大,掌握酸的化学性质(能与活泼金属、金属氧化物、碱、盐等反应)并能灵活运用是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列化学反应及反应类型与如图所示的微观变化对应的是( )
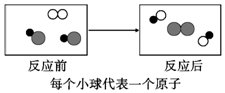

| A. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 化合反应 | |
| B. | 2HI+Cl2═2HCl+I2 置换反应 | |
| C. | 2H2O$\frac{\underline{\;通电\;}}{\;}$ 2H2↑+O2↑ 分解反应 | |
| D. | 2HCl+CuO═CuCl2+H2O 复分解反应 |
1.编制第一个元素周期表的科学家是( )
| A. | 道尔顿 | B. | 卢瑟福 | C. | 门捷列夫 | D. | 汤姆森 |
18.下列关于科学中“不同”的说法中正确的是( )
| A. | H2O与H2O2中氢元素的化合价不同 | |
| B. | O-16与O-18中氧原子的核外电子排布不同 | |
| C. | 镁原子与镁离子的化学性质不同 | |
| D. | 金刚石和石墨的性质差异较大的原因是碳原子的结构不同 |
19.通过对已学知识的对比和归纳,可以得出一些十分有趣的规律.这些规律可以帮助我们掌握学习化学的方法.请你仔细阅读表中的内容,并回答相应的问题.
(1)由表格内容对照可得出的规律是:元素或原子团的化合价数值往往与相应离子所带的电荷数相等;
(2)硫酸亚铁受热能分解,产物均为氧化物,唯一的固体产物呈红色,结合表中信息和反应原理,写出该分解反应产物的化学式:Fe2O3、SO2、SO3;.
| 常见元素或原子团 | OH- | SO42- | CO32- | H元素 | Na元素 | Cl元素 | Fe元素 | S元素 |
| 常见化合价 | -1 | -2 | -2 | +1 | +1 | -1、+5、+7 | +2、+3 | -2、+4、+6 |
(2)硫酸亚铁受热能分解,产物均为氧化物,唯一的固体产物呈红色,结合表中信息和反应原理,写出该分解反应产物的化学式:Fe2O3、SO2、SO3;.

