题目内容
6.已知A、B、C、D、E、F、G是初中化学常见的物质,A在常温下是一种无色液体,D是天然气的主要成分,G是一种重要建筑材料的主要成分,E是一种金属氧化物.它们之间的转换关系如下图所示: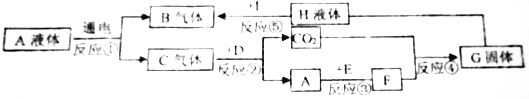
(1)写出下列物质的化学式:AH2OGCaCO3.
(2)写出反应②的化学方程式2O2+CH4$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)反应⑤属于置换反应(填“化合”、“分解”、“置换”)
分析 A在常温下是一种无色液体,通电分解生成B、C两种气体,结合水通电分解生成氢气和氧气,则A为水,B、C两种气体为氢气和氧气中的一种;D是天然气的主要成分,则D为甲烷,甲烷能与氧气在点燃条件下反应生成二氧化碳和水,则C为氧气,B为氢气;G是一种重要建筑材料的主要成分,E是一种金属氧化物,E能与水反应生成G,结合氧化钙与水反应生成氢氧化钙,则E为氧化钙,F为氢氧化钙,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,则G为碳酸钙;碳酸钙能与稀盐酸反应,则H为稀盐酸,稀盐酸与活泼金属反应生成氢气,据此进行分析解答.
解答 解:A在常温下是一种无色液体,通电分解生成B、C两种气体,结合水通电分解生成氢气和氧气,则A为水,B、C两种气体为氢气和氧气中的一种;D是天然气的主要成分,则D为甲烷,甲烷能与氧气在点燃条件下反应生成二氧化碳和水,则C为氧气,B为氢气;G是一种重要建筑材料的主要成分,E是一种金属氧化物,E能与水反应生成G,结合氧化钙与水反应生成氢氧化钙,则E为氧化钙,F为氢氧化钙,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,则G为碳酸钙;碳酸钙能与稀盐酸反应,则H为稀盐酸,稀盐酸与活泼金属反应生成氢气.
(1)A为水,G为碳酸钙,其化学式分别是H2O、CaCO3.
(2)反应②,即甲烷燃烧生成二氧化碳和水,反应的化学方程式为:2O2+CH4$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)反应⑤,即稀盐酸与活泼金属反应生成盐和氢气,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
故答案为:(1)H2O;CaCO3;(2)2O2+CH4$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;(3)置换.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

 目标测试系列答案
目标测试系列答案| A. | 汽油去油污是乳化现象 | |
| B. | 电解水时,常在水中加入氢氧化钠或稀硫酸增强导电性 | |
| C. | 用洗洁精洗涤油腻的碗碟,是利用了溶解的原理 | |
| D. | 电解水产生氢气和氧气,说明水是由氢分子和氧分子构成的 |
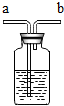
| A. | 实验室中将该装置装满水收集氧气时,气体从b导管进入 | |
| B. | 实验室中将该装置盛浓硫酸干燥氧气时,气体从b导管进入 | |
| C. | 输氧时,a导管连接供给氧气的钢瓶 | |
| D. | 输氧时,该装置也能用来观测氧气输出的速率. |



