题目内容
我校实验室有一瓶保管不当的试剂,其残缺的标签中只剩下“钠”和“10%”字样.已知它是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是 . A、酸 B、碱 C、盐
【查阅资料】Ⅰ、初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.Ⅱ、测定室温(20℃)时,四种物质的溶解度的数据如下:
【得出结论】小华根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是 .
【作出猜想①可能是NaOH溶液;②可能是 溶液;③可能是NaCl.
【设计并实验】
(1)小强取样品少量,滴加无色酚酞试液,液体变红色他认为猜想①正确,他的判断是否合理 ,原因是 .
(2)小华为了检验该溶液到底是什么又进行了如下实验:取样品于试管中,滴加氯化钙溶液,有白色沉淀生成.猜想②正确.相应的化学方程式 .
你还有别的检验方案吗?写出所需试剂及相应的现象(与小华选择试剂种类不能相同). .
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是
【查阅资料】Ⅰ、初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.Ⅱ、测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
【作出猜想①可能是NaOH溶液;②可能是
【设计并实验】
(1)小强取样品少量,滴加无色酚酞试液,液体变红色他认为猜想①正确,他的判断是否合理
(2)小华为了检验该溶液到底是什么又进行了如下实验:取样品于试管中,滴加氯化钙溶液,有白色沉淀生成.猜想②正确.相应的化学方程式
你还有别的检验方案吗?写出所需试剂及相应的现象(与小华选择试剂种类不能相同).
考点:缺失标签的药品成分的探究,溶质的质量分数、溶解性和溶解度的关系,碱的化学性质,盐的化学性质,常见的氧化物、酸、碱和盐的判别
专题:科学探究
分析:【交流讨论】根据酸、碱、盐的组成特点及标签可见部分,猜测该溶液不可能属于哪类物质的溶液;
【得出结论】根据溶液中溶质溶解度与饱和溶液中溶质的质量分数的关系,由常温下各物质的溶解度及该溶液中溶质质量分数,判断溶液的可能性;
【作出猜想】根据提示物质的可能性,对该溶液进行猜想;
【设计并实验】(1)根据三种物质溶液的酸碱性及所测定溶液的酸碱度,对溶液的可能做出判断;
(2)利用碳酸钠、氢氧化钠性质差异及所设计实验中的现象,判断所采取的鉴别所用试剂、现象及结论;
根据碳酸钠、氢氧化钠的性质差异,另选一种试剂完成两种物质的鉴别.
【得出结论】根据溶液中溶质溶解度与饱和溶液中溶质的质量分数的关系,由常温下各物质的溶解度及该溶液中溶质质量分数,判断溶液的可能性;
【作出猜想】根据提示物质的可能性,对该溶液进行猜想;
【设计并实验】(1)根据三种物质溶液的酸碱性及所测定溶液的酸碱度,对溶液的可能做出判断;
(2)利用碳酸钠、氢氧化钠性质差异及所设计实验中的现象,判断所采取的鉴别所用试剂、现象及结论;
根据碳酸钠、氢氧化钠的性质差异,另选一种试剂完成两种物质的鉴别.
解答:解:
【交流讨论】破损标签可见部分为钠元素,可判断该物质由金属元素与根组成,而酸类物质由氢元素与酸根所组成,可判断该物质不可能为酸;
【得出结论】根据常温下碳酸氢钠的溶液为9.6g,可判断常温下碳酸氢钠的饱和溶液的溶质质量分数
×100%=8.8%,因此可判断该溶液不可能为碳酸氢钠溶液;
【作出猜想】除碳酸氢钠外,该溶液可能为氯化钠、碳酸钠或氢氧化钠溶液;
【设计并实验】(1)由于氢氧化钠、碳酸钠溶液都为碱性,能使无色酚酞试液变红色,只有氯化钙溶液显中性,不能使无色酚酞试液变红色,所以不可能是氯化钠溶液;
(2)根据碳酸钠能与氯化钙反应白色碳酸钙沉淀,而与氢氧化钠不能反应而无明显现象,可使用氯化钙溶液鉴别NaOH溶液和Na2CO3溶液;相应的化学方程式:Na2CO3+CaCl2=CaCO3↓+2NaCl;
根据碳酸钠能与稀盐酸放出二氧化碳而氢氧化钠与盐酸反应无明显现象,因此,可推断鉴别两物质时所加入的试剂为稀盐酸,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,观察有气泡可说明该物质为碳酸钠,把产生气体通入澄清石灰水,石灰水会变浑浊.
答案为:
【交流讨论】A
【得出结论】NaHCO3
【作出猜想】Na2CO3
【设计并实验】
(1)不合理 Na2CO3溶液也显碱性
(2)Na2CO3+CaCl2=CaCO3↓+2NaCl
加入稀盐酸,有气泡产生的说明该物质为碳酸钠,无现象的是氢氧化钠
【交流讨论】破损标签可见部分为钠元素,可判断该物质由金属元素与根组成,而酸类物质由氢元素与酸根所组成,可判断该物质不可能为酸;
【得出结论】根据常温下碳酸氢钠的溶液为9.6g,可判断常温下碳酸氢钠的饱和溶液的溶质质量分数
| 9.6g |
| 100g+9.6g |
【作出猜想】除碳酸氢钠外,该溶液可能为氯化钠、碳酸钠或氢氧化钠溶液;
【设计并实验】(1)由于氢氧化钠、碳酸钠溶液都为碱性,能使无色酚酞试液变红色,只有氯化钙溶液显中性,不能使无色酚酞试液变红色,所以不可能是氯化钠溶液;
(2)根据碳酸钠能与氯化钙反应白色碳酸钙沉淀,而与氢氧化钠不能反应而无明显现象,可使用氯化钙溶液鉴别NaOH溶液和Na2CO3溶液;相应的化学方程式:Na2CO3+CaCl2=CaCO3↓+2NaCl;
根据碳酸钠能与稀盐酸放出二氧化碳而氢氧化钠与盐酸反应无明显现象,因此,可推断鉴别两物质时所加入的试剂为稀盐酸,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,观察有气泡可说明该物质为碳酸钠,把产生气体通入澄清石灰水,石灰水会变浑浊.
答案为:
【交流讨论】A
【得出结论】NaHCO3
【作出猜想】Na2CO3
【设计并实验】
(1)不合理 Na2CO3溶液也显碱性
(2)Na2CO3+CaCl2=CaCO3↓+2NaCl
加入稀盐酸,有气泡产生的说明该物质为碳酸钠,无现象的是氢氧化钠
点评:本题综合利用了物质的组成、物质的溶解性、溶液的酸碱性及物质的变化规律对未知物质进行鉴别,体现运用化学知识分析问题、解决问题的能力.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
下列物质的化学式书写正确的是( )
| A、硝酸铵:NH4NO3 |
| B、氧化镁:Mg2O |
| C、碳酸钠:NaCO3 |
| D、氢氧化钙:Ca(HO)2 |
对下列实验中可能会发生的事故处理的方法错误的是( )
| A、如果不慎将碱液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液 |
| B、当酒精洒在桌面上并着火燃烧时,不要惊慌,应立即用湿抹布扑灭 |
| C、如果误饮硫酸铜溶液,应及时饮用生理盐水 |
| D、如果稀酸溅入眼睛,要立即用水冲洗,必要时请医生治疗 |
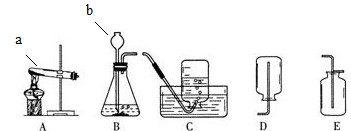
 某兴趣小组利用如图装置进行实验,请回答:
某兴趣小组利用如图装置进行实验,请回答:
