题目内容
14.氢气还原氧化铜生成红色固体,这些红色固体是什么物质?某科学兴趣小组查阅资料得知,反应温度不同,氢气还原氧化铜的产物可能是Cu或Cu2O,Cu和Cu2O均为不溶于水的红色固体:但氧化亚铜能与稀硫酸反应,化学方程式为:Cu2O+H2SO4═CuSO4+Cu+H2O.为探究反应后红色固体中含有什么物质?它们提出了以下假设:假设一:红色固体只有Cu
假设二:红色固体只有Cu2O
假设三:红色固体中有Cu和Cu2O
请回答有关问题.
(1)取少量红色固体,加入足量的稀硫酸.若无明显现象,则假设一成立;
(2)现将3克红色固体加入足量的稀硫酸中,反应后的溶液过滤,称得烘干后的滤渣质量为1.4克,则原红色固体中含有什么物质?Cu和Cu2O.
分析 根据实验现象可以判断物质的组成情况;
通过计算可以判断原红色固体中含有什么物质.
解答 解:(1)取少量红色固体,加入足量的稀硫酸,若无明显现象,说明红色固体中不含有氧化亚铜,假设一成立.
故答案为:一.
(2)假设3克红色固体中只含有氧化亚铜,设氧化亚铜和稀硫酸反应生成铜的质量为x,
Cu2O+H2SO4═CuSO4+Cu+H2O
144 64
3g x
$\frac{144}{3g}=\frac{64}{x}$
x=1.3g,
由计算可知,假设不成立,所以原红色固体中含有铜和氧化亚铜.
故答案为:
(1)一;
(2)Cu和Cu2O.
点评 计算时,可以假设3克红色固体是氧化亚铜,计算生成铜的质量,再和烘干后的滤渣质量为1.4克相比较,便可得出正确的结论.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
5.下列化学方程式书写正确的是( )
| A. | Fe2O3+4HCl═2FeCl2+2H2O | B. | Al(OH)3+3HCl═AlCl3+3H2O | ||
| C. | Cu+H2SO4═H2↑+CuSO4 | D. | KNO3+NaCl═KCl↓+NaNO3 |
9.建立模型是学习科学的重要方法,在理解化学反应的本质时往往引入模型.如图是某反应的微观模型,有关该模型的叙述中,正确的是( )
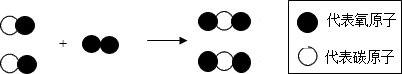

| A. | 该反应是分解反应 | B. | 反应前后原子种类发生改变 | ||
| C. |  相对分子质量为44g 相对分子质量为44g | D. |  是保持氧气化学性质的微粒 是保持氧气化学性质的微粒 |
19.下列对有关反应的描述正确的是( )
| A. | 镁带在空气中剧烈燃烧,发出耀眼的白光,生成白色固体 | |
| B. | 在点燃的条件下,磷在氧气中剧烈燃烧,产生大量白雾 | |
| C. | 在点燃的条件下,硫在氧气里燃烧,发出蓝紫色火焰,生成无色无味的气体 | |
| D. | 在点燃的条件下,细铁丝在氧气中剧烈燃烧,火星四射,生成黑色的三氧化二铁 |
6.区分下列各组物质的两种方法都合理的是( )
| 选项 | 需区分的物质 | 方法一 | 方法二 |
| A | 硬水和软水 | 观察是否澄清 | 加肥皂水搅拌 |
| B | 氧气和二氧化碳 | 观察颜色 | 加入澄清石灰水 |
| C | 硫磺和红磷 | 观察颜色 | 在氧气中点燃后观察现象 |
| D | 黄铜(铜锌合金)和黄金 | 分别滴加硫酸锌溶液 | 加热后观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
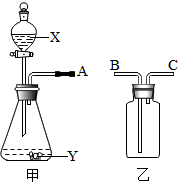 如图是实验常用的气体制备、收集、净化的两种多功能装置.
如图是实验常用的气体制备、收集、净化的两种多功能装置. 已知X是有毒且不溶于水的气体,Y是不支持燃烧的气体,Z是不溶于水的固体,X、Y、Z之间有如图转化关系.请回答下列问题:
已知X是有毒且不溶于水的气体,Y是不支持燃烧的气体,Z是不溶于水的固体,X、Y、Z之间有如图转化关系.请回答下列问题: